
发布时间:2021-01-08
附件:总胆汁酸测定试剂注册技术审查指导原则(2020年第14号).doc
本指导原则旨在指导注册申请人对总胆汁酸(Total bile acids,TBA)测定试剂注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。
本指导原则是对总胆汁酸测定试剂的一般要求,申请人应依据产品的具体特性确定其中的具体内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特征对注册申报资料的内容进行充实和细化。
本指导原则是供申请人和审查人员适用的指导文件,不涉及注册审批等行政事项,亦不作为法规强制执行,如果有能够满足相关法规要求的其他方法,也可以采用,但应提供详细的研究资料和验证资料。应在遵循相关法规、国家标准、行业标准的前提下使用本指导原则。
本指导原则是在现行法规、标准体系及当前认知水平下制定的,随着法规、标准体系的不断完善和科学技术的不断发展,本指导原则相关内容也将适时进行调整。
一、适用范围
本指导原则适用于基于采用3α-羟基类固醇脱氢酶(3α-HSD)催化的酶促循环反应(酶循环法)原理,利用全自动生化分析仪、半自动生化分析仪或分光光度计,体外定量测定人血清或血浆中总胆汁酸含量的试剂盒。本指导原则适用于进行首次注册申报和相关许可事项变更的产品。
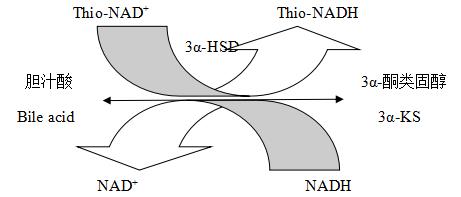
反应原理如图所示。胆汁酸被3α-HSD及β-硫代氧化型烟酰胺腺嘌呤二核苷酸(Thio-NAD+)特异性地氧化,生成3α-酮类固醇(3α-KS)及β-硫代还原型烟酰胺腺嘌呤二核苷酸(Thio-NADH)。此外,生成的3α-KS在3α-HSD及还原型辅酶I(NADH)存在下,又生成胆汁酸和氧化型辅酶I(NAD+)。这样,血清或血浆中微量的胆汁酸在多次酶循环的过程中被放大,同时可使生成的Thio-NADH扩增,其扩增速率与胆汁酸的含量相关。通过测定Thio-NADH在405nm波长附近吸光度的变化率,从而计算出血清或血浆中胆汁酸的含量。
依据《体外诊断试剂注册管理办法》(国家食品药品监督管理总局令第5号,以下简称《办法》)、《食品药品监管总局关于印发体外诊断试剂分类子目录的通知》(食药监械管〔2013〕242号),总胆汁酸检测试剂盒属于用于其他生理、生化或免疫功能指标检测的检测试剂,管理类别为二类,分类代码为6840。
二、注册申报资料要求
(一)综述资料
综述资料主要包括产品预期用途、产品描述、有关生物安全性方面的说明、研究结果总结以及同类产品上市情况介绍等内容,应符合《体外诊断试剂注册管理办法》和《关于公布体外诊断试剂注册申报资料要求和批准证明文件格式的公告》(国家食品药品监督管理总局公告2014年第44号)的相关要求。相关描述应至少包含如下内容:
1.产品预期用途及相关的临床适应症背景情况
1.1总胆汁酸测定试剂用于体外定量测定血清或血浆中总胆汁酸的含量。
1.2总胆汁酸的生物学特征、结构与功能,在体内正常和病理状态下的代谢途径和存在形式。
1.3与预期用途相关的临床适应症背景情况,如临床相关疾病的发生、实验室诊断方法等。
2.产品描述:包括产品所采用的技术原理,主要原材料的来源及制备方法,主要生产工艺过程,校准品的制备方法及溯源情况(如需提供)、质控品的制备方法及定值情况(如需提供)。
3.有关生物安全性方面的说明:由于体外诊断试剂中的主要原材料可能是由各种动物、病原体、人源的组织和体液等生物材料经处理或添加某些物质制备而成,人源性材料须对有关传染病(HIV、HBV、HCV等)病原体检测予以说明,并提供相关的证明文件,其他动物源及微生物来源的材料,应当提供相应的说明文件。为保证产品在运输、使用过程中对使用者和环境的安全,应提供对上述原材料所采用的灭活等试验方法的说明。
4.有关产品主要研究结果的总结和评价。
5.其他:包括同类产品在国内外批准上市的情况。相关产品所采用的技术方法及临床应用情况,申请注册产品与国内外同类产品的异同等。
(二)主要原材料的研究资料(如需提供)
包括主要反应成分、质控品(如适用)、校准品(如适用)等的选择、制备、质量标准确定的方法及研究资料;校准品应提供详细的量值溯源资料,包括定值试验资料和溯源性文件等;质控品应提供详细的定值资料。
(三)主要生产工艺和反应体系的研究资料(如需提供)
主要工艺包括:配制、分装、冻干等描述及确定依据,应包含产品的工艺流程图和关键控制点;反应体系包括样本采集及处理、样本要求、试剂用量、反应条件(温度、时间等)等。不同适用机型的反应条件如果有差异应分别详述。
(四)分析性能评估资料
申请人应当提交不少于3批产品的全部分析性能评估资料,对于每项分析性能的评估都应包括具体的研究项目、实验设计、研究方法、可接受标准、试验数据、统计方法、研究结论等详细资料。性能评估时应将试剂和所选用的校准品、质控品作为一个整体进行评价,评估整个系统的性能是否符合要求。有关分析性能验证的背景信息也应在申报资料中有所体现,包括实验时间、地点、检验人员、适用仪器、试剂规格和批号、所选用的校准品和质控品(品牌、规格、批号等)、临床样本来源等。
对于TBA定量测定试剂,分析性能评估应至少包括试剂空白吸光度、试剂空白吸光度变化率、准确度、精密度、线性区间、分析灵敏度、分析特异性等性能指标。干粉或冻干试剂还应包括批内瓶间差。
1.空白吸光度
用指定空白样本测试试剂盒,在405nm 波长附近、1cm光径条件下,记录测试启动时的吸光度(A1),扣除反应的非线性段或约5 分钟(T)后的吸光度(A2),A2测试结果即为试剂空白吸光度测定值,结果均值应符合产品技术要求性能指标的要求。
2.试剂空白吸光度变化率
记录测试启动时的吸光度(A1),扣除反应的非线性段或约5分钟(T)后的吸光度(A2),计算出吸光度变化值(|A2-A1|/T),即为试剂空白吸光度变化率((A/min),结果应符合产品技术要求性能指标的要求。
3.准确度
对测量准确度的评价依次包括:与国家参考物(和/或国际参考物)的偏差分析、回收试验、方法学比对等方法,申请人可根据实际情况选择合理方法进行研究。
3.1与国家参考物(和/或国际参考物)的偏差分析
用有证参考物质(CRM)或其他公认的参考物质或由参考方法定值的高、低2个浓度的人源样品,对试剂盒进行测试,重复测定3次,取测试结果均值(M),根据公式(1)计算相对偏差。如果3次结果都符合规定,即判为合格;如果大于等于2次的结果不符合,即判为不合格;如果有1次结果不符合规定,则应重新连续测试20次,分别计算相对偏差,如果大于等于19次测试的结果符合规定,即判为合格......

站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。
ONE-STOP SERVICE
免费赠送3万家医疗器械企业名录