
发布时间:2020-12-22
根据《深度学习辅助决策医疗器械软件审评要点》的要求,从临床试验的角度出发,人工智能(AI)医疗软件产品仍然归类为“诊断产品”,其临床试验本质上仍然是一个诊断试验,因此,在试验设计上具有传统诊断试验的相似特征。

若AI医疗软件针对的疾病而不涉及病灶的定位要求(如糖网诊断只需要知道患者是否患病就足够了),则其临床试验的设计较为简单,采用传统的诊断试验设计即可;若AI医疗软件针对的疾病具有病灶的定位要求(如CT影像中的肺结节的识别及定位、内镜影像下对息肉的识别及定位等),则其临床试验与传统的诊断试验设计将存在一定的差别,包括灵敏度的定义、ROC曲线的绘制、非完美金标准的校正等等,所以根据所用的适应症(是否为急症)、产品的性能及临床价值以及风险级别不同,所采用的设计类型也有所差别。
对于安全级别为B、A级的中低风险医疗软件,回顾性研究可用作临床预实验或替代临床试验,而安全级别为C级的高风险软件,回顾性研究可作为预实验,为临床试验设计提供参考依据。另外C级别高风险软件:适用范围变更应当开展临床试验,其他情况原则上可使用回顾性研究。
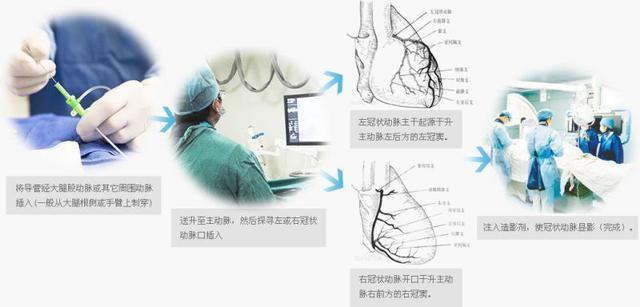
以冠脉CT造影图像血管狭窄辅助分诊软件临床试验为例,其临床应用要求仅仅需要保证分诊提示准确率,在满足临床工作需求的基础上,可以大幅缩短阅片时间,减轻临床医师工作量。但由于该产品不能用于急性冠脉综合征(ACS)等急性胸痛患者,仅供经培训合格的医师使用,不能单独用作临床诊疗决策依据,因此风险级别有所降低,该案例完全采用回顾性试验设计,而获得审批通过,是探索性使用回顾性试验设计完成AI软件注册的一个成功案例。
虽然法规认为中低风险级别AI软件可以采用回顾性设计,但是由于回顾性研究存在诸多难以避免的严重偏倚,包括测量偏倚、临床参考标准偏倚(回顾性受试者病历收集不全面)、选择偏倚(如临床试验仅选择了具有金标准诊断(如组织活检)的患者作为阳性病例,而接受了金标准诊断的病例往往是严重且典型的)等。且实际应用存在评价偏倚,需要有严格控制偏倚的措施,以降低对试验造成的影响才能使用,因此AI软件类产品临床试验应当慎重选用回顾性设计。
来源:CIRS

站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。
ONE-STOP SERVICE
免费赠送3万家医疗器械企业名录