
发布时间:2026-05-14
第一章药品注册申请受理情况
(一)总体情况
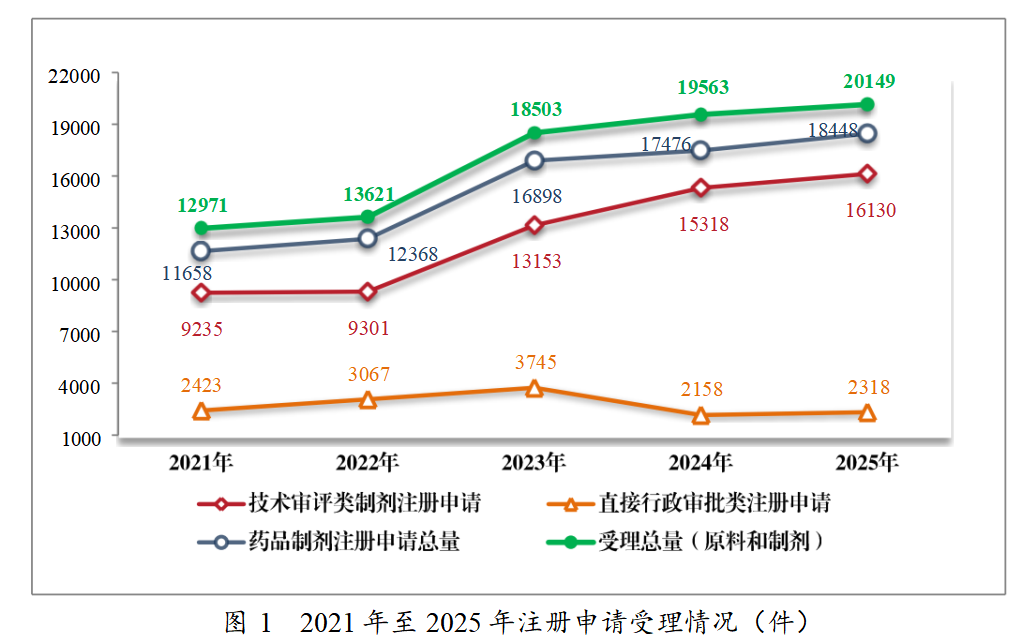
2025 年,药品注册申请申报量持续增长,药审中心受理各类注册申请20149 件(同比增加3.00%,以受理号计,下同),包括药品制剂注册申请18448 件(同比增加5.56%),化学原料药注册申请1701 件。18448 件药品制剂注册申请包括技术审评类注册申请16130 件(同比增加5.30%),直接行政审批类注册申请2318 件(包括补充申请和一次性进口)。2021 年至2025 年注册申请受理情况详见图1。
(二)技术审评类药品注册申请受理情况
2025年受理 16130件技术审评类药品注册申请,以药品类型统计,中药注册申请2723件,化学药品注册申请10587件,生物制品注册申请2820 件。2021 年至2025 年需技术审评的各药品类型注册申请受理情况详见图2。

以注册申请类别统计,受理临床试验申请3756件,新药上市许可申请(该注册申请类别以下简称“NDA”)663 件,同名同方药、化学仿制药上市许可申请(该注册申请类别以下简称“ANDA”)4591件,仿制药质量和疗效一致性评价注册申请(该注册申请类别以下简称“一致性评价申请”)430 件,补充申请6293 件,境外生产药品再注册申请397 件。2021 年至2025 年需技术审评的各类别注册申请受理情况详见图3。

1.中药注册申请受理情况
2025 年受理中药注册申请2723 件,按注册申请类别统计,临床试验申请140 件,NDA54 件,ANDA 11 件,补充申请2488 件,境外生产药品再注册申请30件。2021年至2025年需技术审评的中药各类别注册申请受理情况详见图4。

以注册分类统计,140 件临床试验申请包括创新中药临床试验申请103 件(89 个品种),改良型中药临床试验申请36 件(30 个品种),同名同方药临床试验申请 1件(1个品种);54件NDA包括创新中药NDA 14 件(13 个品种),改良型中药NDA4 件(4 个品种),古代经典名方中药复方制剂NDA 36 件(24 个品种)。
2025 年各注册分类中药临床试验申请、NDA 受理情况详见表1,2021年至2025年各注册分类中药临床试验申请受理情况详见图5,2021 年至2025 年各注册分类中药NDA受理情况详见图6。
表1 2025 年各注册分类中药临床试验申请、NDA受理情况
|
注册 申请 类别 |
注册分类 |
中药 |
||||
|
注册申请(件) |
品种(个) |
|||||
|
临床试验申请 |
创新药 |
1.1 |
82 |
79 |
||
|
1.2 |
21 |
10 |
||||
|
改良型新药 |
2.1 |
2 |
1 |
|||
|
2.1;2.3 |
1 |
1 |
||||
|
2.2 |
4 |
4 |
||||
|
2.3 |
25 |
23 |
||||
|
2.4 |
4 |
1 |
||||
|
同名同方药 |
4 |
1 |
1 |
|||
|
合计 |
140 |
120 |
||||
|
NDA |
创新药 |
1.1 |
12 |
12 |
||
|
1.2 |
2 |
1 |
||||
|
改良型新药 |
2.1 |
1 |
1 |
|||
|
2.2 |
1 |
1 |
||||
|
2.3 |
2 |
2 |
||||
|
古代经典名方 |
3.1 |
36 |
24 |
|||
|
合计 |
54 |
41 |
||||
|
总计 |
194 |
161 |
||||


2.化学药品注册申请受理情况
2025 年受理化学药品注册申请10587 件,按注册申请类别统计,临床试验申请2187 件,NDA310 件,ANDA4580 件,一致性评价申请430 件,补充申请2768 件,境外生产药品再注册申请312 件。2021年至2025年需技术审评的化学药品各类别注册申请受理情况详见图7。

以注册分类统计,2187 件临床试验申请包括创新化学药品临床试验申请1470件(606个品种),改良型化学药品临床试验申请466件(256个品种),化学药品5.1类临床试验申请 11件(7个品种),仿制药临床试验申请240 件;310 件NDA 包括创新化学药品NDA86件(52个品种),改良型化学药品NDA131件(68个品种),5.1类化学药品NDA 93 件(57 个品种)。
2025 年各注册分类化学药品临床试验申请、NDA受理情况详见表2,2021年至2025年各注册分类化学药品临床试验申请受理情况详见图8,2021年至2025年各注册分类化学药品NDA受理情况详见图9。
表2 2025 年各注册分类化学药品临床试验申请、NDA受理情况
|
注册申请类别 |
注册分类 |
化学药品 |
||
|
注册申请(件) |
品种(个) |
|||
|
临床试验申请 |
创新药 |
1 |
1470 |
606 |
|
改良型新药 |
2.1 |
6 |
5 |
|
|
2.1;2.2 |
7 |
4 |
||
|
2.1;2.2;2.4 |
3 |
2 |
||
|
2.1;2.4 |
3 |
2 |
||
|
2.2 |
218 |
122 |
||
|
2.2;2.4 |
55 |
30 |
||
|
2.3 |
30 |
20 |
||
|
2.4 |
144 |
71 |
||
|
境外上市原研药和改良型药品 |
5.1 |
11 |
7 |
|
|
合计 |
1947 |
869 |
||
|
NDA |
创新药 |
1 |
86 |
52 |
|
改良型新药 |
2.1;2.2 |
1 |
1 |
|
|
2.1;2.2;2.4 |
1 |
1 |
||
|
2.2 |
54 |
23 |
||
|
2.2;2.4 |
3 |
3 |
||
|
2.3 |
9 |
7 |
||
|
2.4 |
63 |
33 |
||
|
境外上市原研药 |
5.1 |
93 |
57 |
|
|
注册申请类别 |
注册分类 |
化学药品 |
||
|
注册申请(件) |
品种(个) |
|||
|
和改良型药品 |
||||
|
合计 |
310 |
177 |
||
|
总计 |
2257 |
1046 |
||
注:部分注册申请同时符合《化学药品注册分类及申报资料要求》中的多个类别,故申请人同时填写了多个注册分类信息。未包含仿制药临床试验申请。

3.生物制品注册申请受理情况
2025 年受理生物制品注册申请2820 件,包括预防用生物制品注
册申请191件、治疗用生物制品注册申请2620件和体外诊断试剂注册申请9 件。
按注册申请类别统计,临床试验申请1429 件,NDA 299 件,补充申请1037 件,境外生产药品再注册申请55 件。2021年至2025 年需技术审评的生物制品各类别注册申请受理情况详见图10。

以注册分类统计,102 件预防用生物制品临床试验申请包括创新型疫苗临床试验申请 61件(43个品种),改良型疫苗临床试验申请15件(11个品种),境内或境外已上市疫苗临床试验申请26件(16个品种);21件预防用生物制品NDA包括创新型疫苗NDA4件(3个品种),改良型疫苗NDA3 件(2 个品种),境内或境外已上市疫苗NDA14 件(10个品种)。
2025 年各注册分类预防用生物制品临床试验申请、NDA受理情况详见表3,2021年至2025年各注册分类预防用生物制品临床试验申请受理情况详见图11,2021 年至2025 年各注册分类预防用生物制品NDA受理情况详见图12。
表3 2025 年各注册分类预防用生物制品临床试验申请、NDA受理情况
|
注册申 请类别 |
注册分类 |
预防用生物制品 |
||
|
注册申请(件) |
品种(个) |
|||
|
临床试验申请 |
创新型疫苗 |
1.1 |
6 |
6 |
|
1.2 |
33 |
21 |
||
|
1.3 |
14 |
9 |
||
|
1.4 |
8 |
7 |
||
|
改良型疫苗 |
2.2 |
11 |
8 |
|
|
2.5 |
3 |
2 |
||
|
2.6 |
1 |
1 |
||
|
境内或境外已上市疫 苗 |
3.1 |
4 |
4 |
|
|
3.2 |
7 |
5 |
||
|
3.3 |
15 |
7 |
||
|
合计 |
102 |
70 |
||
|
NDA |
创新型疫苗 |
1.2 |
1 |
1 |
|
1.3 |
2 |
1 |
||
|
1.4 |
1 |
1 |
||
|
改良型疫苗 |
2.1 |
1 |
1 |
|
|
2.2 |
2 |
1 |
||
|
境内或境外已上市疫 苗 |
3.1 |
2 |
1 |
|
|
3.2 |
1 |
1 |
||
|
3.3 |
11 |
8 |
||
|
合计 |
21 |
15 |
||
|
总计 |
126 |
82 |
||


以注册分类统计,1327 件治疗用生物制品临床试验申请包括创新治疗用生物制品临床试验申请1073 件(674 个品种),改良型治疗用生物制品临床试验申请192 件(85 个品种),境内或境外已上市治疗用生物制品临床试验申请62 件(47 个品种)。
272件治疗用生物制品NDA包括创新治疗用生物制品NDA50件(35个品种),改良型治疗用生物制品NDA89件(36个品种),境内或境外已上市治疗用生物制品NDA133 件(60 个品种)。
2025 年各注册分类治疗用生物制品临床试验申请、NDA受理情况详见表4,2021年至2025年各注册分类治疗用生物制品临床试验申请受理情况详见图13,2021 年至2025 年各注册分类治疗用生物制品NDA受理情况详见图14。
表4 2025 各注册分类治疗用生物制品临床试验申请、NDA受理情况
|
注册申请类别 |
注册分类 |
治疗用生物制品 |
||
|
注册申请(件) |
品种(个) |
|||
|
临床试验申请 |
创新型生物制品 |
1 |
1073 |
674 |
|
改良型生物制品 |
2.1 |
18 |
13 |
|
|
2.1;2.2 |
6 |
3 |
||
|
2.1;2.3 |
2 |
1 |
||
|
2.2 |
153 |
61 |
||
|
2.2;2.4 |
4 |
2 |
||
|
2.4 |
9 |
5 |
||
|
境内或境外已上市生物制品 |
3.1 |
5 |
5 |
|
|
3.2 |
8 |
6 |
||
|
3.3 |
41 |
29 |
||
|
3.4 |
8 |
7 |
||
|
合计 |
1327 |
806 |
||
|
NDA |
创新型生物制品 |
1 |
50 |
35 |
|
改良型生物制品 |
2.1 |
27 |
3 |
|
|
2.1;2.2 |
1 |
1 |
||
|
2.2 |
60 |
31 |
||
|
2.4 |
1 |
1 |
||
|
境内或境外已上市生物制品 |
3.1 |
68 |
28 |
|
|
3.2 |
8 |
7 |
||
|
3.3 |
44 |
14 |
||
|
3.4 |
13 |
11 |
||
|
合计 |
272 |
131 |
||
|
总计 |
1599 |
937 |
||


(三)直接行政审批类注册申请受理情况
2025 年受理直接行政审批类注册申请2318 件,包括无需技术审评的补充申请1927 件,临时进口注册申请391 件。2021 年至2025 年直接行政审批的各类别注册申请受理情况详见图15。

第二章药品注册申请审评审批情况
(一)总体情况
2025年,药审中心审结各类药品注册申请共 19375件(同比增加6.11%),包括药品制剂注册申请17679 件(同比增加9.69%),化学原料药注册申请 1696件。17679件药品制剂注册申请包含技术审评类注册申请15408 件(同比增加 10.75%),直接行政审批类注册申请2271 件。2021 年至2025年药品注册申请审结量详见图16。

截至2025 年底,在审和待审的药品注册申请共12291 件,其中包含原料药注册申请2393 件;待申请人回复补充资料的注册申请共3033 件,其中包含原料药注册申请640 件。
(二)技术审评类药品注册申请审结情况
2025年审结 15408件技术审评类药品注册申请,以药品类型统计,中药注册申请2439件,化学药品注册申请10297件,生物制品注册申请2672件。2021年至2025年需技术审评的各药品类型注册申请审结情况详见图17。

以注册申请类别统计,2025 年审结临床试验申请3773 件,NDA562 件,ANDA4215 件,一致性评价申请660 件,补充申请5865 件,境外生产药品再注册申请333 件。2021 年至2025 年需技术审评的各类别注册申请审结情况详见图18。

2025 年,药审中心以临床价值为导向,采取多种措施提高审评效率,加快新药好药上市,为患者提供更多的用药选择。
按照我国药品注册分类相关标准,全年批准上市1类创新药 76个品种(详见附件1),其中26 个品种(34.2%)通过优先审评审批程序批准上市,15个品种(19.7%)附条件批准上市,15个品种(19.7%)在临床试验期间纳入了突破性治疗药物程序。
全年批准罕见病用药48个品种(未包括化学药品4类仿制药),其中12 个品种(24.5%)通过优先审评审批程序加快上市(详见附件2)。
全年批准儿童用药138个品种,包含98个上市许可申请,其中25个品种(18.1%)通过优先审评审批程序加快上市(详见附件3);另批准40 个品种扩展儿童适应症。
全年批准放射性药品6个品种,其中3个品种(50.0%)通过优先审评审批程序加快上市。
全年批准境外已上市境内未上市的药品(化学药品5.1类、治疗用生物制品3.1类和预防用生物制品3.1类)80个品种,其中 57个为首次批准上市,23 个为已上市药品增加适应症,详见附件4。
1.中药注册申请审结情况
2025 年审结中药注册申请2439 件,按注册申请类别统计,临床试验申请137 件,NDA39 件,ANDA4 件,补充申请2246 件,境外生产药品再注册申请13 件。2025 年中药各类别注册申请审结情况详见表5。
表5 2025 年需技术审评的中药注册申请审结情况(件)
|
注册申请类别 |
审结量 |
|||
|
批准/审评通过 |
不批准 /审评不通过 |
其他 |
合计 |
|
|
临床试验申请 |
115 |
0 |
22 |
137 |
|
NDA |
24 |
4 |
11 |
39 |
|
ANDA |
1 |
0 |
3 |
4 |
|
补充申请 |
2010 |
33 |
203 |
2246 |
|
境外生产药品再注册 申请 |
13 |
0 |
0 |
13 |
|
总计 |
2163 |
37 |
239 |
2439 |
注:“其他”是指申请人未按规定缴纳费用、撤回申请等原因导致审评审批终止的情形。
批准中药临床试验申请115 件(102 个品种),以注册分类统计,包括创新中药临床试验申请 89件(78个品种),改良型中药临床试验申请25件(23个品种),同名同方药临床试验申请1件(1个品种);审评通过中药NDA24 件(24 个品种),以注册分类统计,包括创新中药NDA5 件(5 个品种),改良型中药NDA3 件(3 个品种),古代经典名方中药复方制剂NDA16 件(16 个品种)。
2025 年各注册分类中药临床试验申请、NDA批准/审评通过情况详见表6,2021年至2025年各注册分类中药临床试验申请批准情况详见图19,2021年至2025年各注册分类中药NDA、ANDA审评通过情况详见图20。
表6 2025 年各注册分类中药临床试验申请、NDA 批准/审评通过量
|
注册申请类别 |
注册分类 |
中药 |
||
|
注册申请(件) |
品种(个) |
|||
|
临床试验申请 |
创新药 |
1.1 |
73 |
70 |
|
1.2 |
16 |
8 |
||
|
改良型新药 |
2.1;2.3 |
1 |
1 |
|
|
2.2 |
4 |
4 |
||
|
2.3 |
20 |
18 |
||
|
同名同方药 |
4 |
1 |
1 |
|
|
合计 |
115 |
102 |
||
|
NDA |
创新药 |
1.1 |
5 |
5 |
|
改良型新药 |
2.1 |
1 |
1 |
|
|
2.2 |
1 |
1 |
||
|
2.3 |
1 |
1 |
||
|
古代经典名方 |
3.1 |
16 |
16 |
|
|
合计 |
24 |
24 |
||
|
总计 |
总计 |
139 |
126 |
|


批准的 115件中药临床试验申请涉及 13个适应症领域,其中呼吸、精神神经较多,占中药临床试验申请批准量的33.04%。2025年批准中药临床试验申请的适应症领域分布情况详见图21。

审评通过的中药NDA24 件涉及7 个适应症领域,其中呼吸、消化药物较多,占中药NDA审评通过量的45.83%。2025年审评通过中药NDA的适应症领域分布情况详见图22。

2.化学药品注册申请审结情况
2025 年审结化学药品注册申请10297 件,按注册申请类别统计,临床试验申请2251 件,NDA282 件,ANDA4211 件,一致性评价申请660 件,补充申请2617 件,境外生产药品再注册申请276 件。2025
年化学药品各类别注册申请审结情况详见表7。
表7 2025 年需技术审评的化学药品注册申请审结情况(件)
|
注册申请类别 |
审结量 |
|||
|
批准/审评 通过 |
不批准 /审评不通过 |
其他 |
合计 |
|
|
临床试验申请 |
2144 |
12 |
95 |
2251 |
|
NDA |
251 |
10 |
21 |
282 |
|
ANDA |
3651 |
164 |
396 |
4211 |
|
一致性评价申请 |
603 |
12 |
45 |
660 |
|
补充申请 |
2347 |
59 |
211 |
2617 |
|
境外生产药品再注册申请 |
274 |
0 |
2 |
276 |
|
总计 |
9270 |
257 |
770 |
10297 |
(1)新药临床试验申请和新药上市申请
批准化学药品临床试验申请 2144 件,以注册分类统计,包括创新化学药品临床试验申请1438 件(610 个品种),改良型化学药品临床试验申请437件(251个品种),化学药品5.1类临床试验申请 12件(9个品种),仿制药临床试验申请257 件;审评通过化学药品NDA251 件(149 个品种),以注册分类统计,包括创新化学药品NDA 93件(55 个品种),改良型化学药品NDA71 件(39个品种),5.1类化学药品NDA 87 件(55 个品种)。
2025 年各注册分类化学药品临床试验申请、NDA 批准/审评通过情况详见表8,2021年至2025年各注册分类化学药品临床试验申请批准情况详见图23,2021 年至2025 年各注册分类化学药品NDA审评通过情况详见图24。
表8 2025 年各注册分类化学药品临床试验申请、NDA 批准/审评通过情况
|
注册申请类别 |
注册分类 |
化学药品 |
||
|
注册申请(件) |
品种(个) |
|||
|
临床试验申请 |
创新药 |
1 |
1438 |
610 |
|
改良型新药 |
2.1 |
7 |
4 |
|
|
2.1;2.2 |
5 |
3 |
||
|
2.1;2.2;2.4 |
7 |
5 |
||
|
2.1;2.4 |
4 |
2 |
||
|
2.2 |
204 |
117 |
||
|
2.2;2.4 |
38 |
27 |
||
|
2.3 |
24 |
18 |
||
|
2.3;2.4 |
1 |
1 |
||
|
2.4 |
147 |
74 |
||
|
境外上市原研 药和改良型药 品 |
5.1 |
12 |
9 |
|
|
合计 |
1887 |
870 |
||
|
NDA |
创新药 |
1 |
93 |
55 |
|
改良型新药 |
2.2 |
21 |
12 |
|
|
2.2;2.4 |
2 |
2 |
||
|
2.3 |
4 |
4 |
||
|
2.4 |
44 |
21 |
||
|
境外上市原研 药和改良型药 品 |
5.1 |
87 |
55 |
|
|
合计 |
251 |
149 |
||
|
总计 |
2138 |
1019 |
||
注:未包含仿制药临床试验申请


批准的化学药品(仿制药除外)临床试验申请 1887件中,抗肿瘤药物占37.10%、皮肤及五官科药物占9.17%,内分泌系统疾病药物和循环系统疾病药物各占8.21%。2025 年批准化学药品临床试验申请的适应症领域分布情况详见图25。

审评通过的化学药品NDA251 件中,抗肿瘤药物占34.66%、精神障碍疾病药物占 11.16%,内分泌系统疾病药物占9.96%。2025年审评通过化学药品NDA的适应症领域分布情况详见图26。

(2)化学仿制药上市申请
2025 年审评通过化学仿制药上市申请3650 件,有效满足了临床患者对高质量仿制药的需求。化学药品注册分类改革以来,按照与原研药品质量和疗效一致性的要求,累计审评通过化学仿制药11227 件,涉及循环系统疾病药物、抗感染药物等17 个治疗领域,具体见图27。

为落实《国务院办公厅关于进一步做好短缺药品保供稳价工作的意见》,2020 年,国家卫生健康委等十二部门联合发布了国家短缺药品清单和临床必需易短缺药品重点监测清单。2025 年,共审评通过两个清单内的短缺药品174 件(33 个品种)。近五年累计审评通过短缺药品共396 件(43 个品种),见图28,涉及循环系统疾病药物、神经系统疾病药物、抗肿瘤药物等13 个治疗领域,具体见图29,有效保障了短缺药品的供应。


为进一步促进儿童适宜品种、剂型、规格的研发创制和申报审评,满足儿科临床用药需求,自2016年起,国家卫生健康委会同有关部门研究制订了五批鼓励研发申报儿童药品清单,共有160 个品种,包括口服溶液剂、口服混悬剂、颗粒剂等适宜儿童给药剂型。2025 年,审评通过清单内的鼓励研发申报儿童药品15 件(8 个品种)。近五年累计审评通过鼓励研发申报儿童药品63件(31个品种),见图 30,涉及神经系统疾病药物、精神障碍疾病药物、镇痛药及麻醉科用药等12 个治疗领域,具体涉及适应症情况请见图31。

(3)化学仿制药质量和疗效一致性评价工作
2025 年,药审中心持续推进化学仿制药质量和疗效一致性评价工作,共发布参比制剂目录 13批,涉及883个品规(521个品种)。截至2025 年12月31 日,累计发布参比制剂目录100批,共8526 个品规(2859 个品种)。
2025年批准一致性评价申请603件(227个品种),其中,口服固体制剂146件(103个品种),注射剂457件(124个品种)。自化学仿制药质量和疗效一致性评价工作开展以来,累计批准一致性评价申请共5406 件(共计805 个品种),其中,口服固体制剂2283 件(计489 个品种),注射剂3123 件(计316 个品种)。2021 年至2025年一致性评价申请批准情况详见图32。

3.生物制品注册申请审结情况
2025 年,审结生物制品注册申请2672 件,包括预防用生物制品214 件,治疗用生物制品2453 件和体外诊断试剂5 件。
按注册申请类别统计,临床试验申请1385 件,NDA 241 件,补充申请 1002件,境外生产药品再注册申请44件。2025年生物制品各类别注册申请审结情况详见表9。
表9 2025 年需技术审评的生物制品注册申请审结情况(件)
|
注册申请类别 |
审结量 |
|||
|
批准/审评通过 |
不批准 /审评不通过 |
其他 |
合计 |
|
|
预防用生物制品临床试验申请 |
87 |
0 |
13 |
100 |
|
治疗用生物制品临床试验申请 |
1220 |
7 |
58 |
1285 |
|
预防用生物制品NDA |
17 |
0 |
0 |
17 |
|
治疗用生物制品NDA |
202 |
1 |
20 |
223 |
|
体外诊断试剂NDA |
0 |
0 |
1 |
1 |
|
补充申请 |
928 |
0 |
74 |
1002 |
|
境外生产药品再注册 申请 |
42 |
0 |
2 |
44 |
|
总计 |
2496 |
8 |
168 |
2672 |
(1)预防用生物制品
批准预防用生物制品临床试验申请87件,以注册分类统计,包括创新型疫苗临床试验申请 57件(40个品种),改良型疫苗临床试验申请10 件(7个品种),境内或境外已上市疫苗20 件(14个品种);审评通过预防用生物制品NDA 17 件(12 个品种),以注册分类统计,包括创新型疫苗NDA 1 件(1 个品种),改良型疫苗NDA3 件(2 个品种),境内或境外已上市疫苗NDA13 件(9 个品种)。
2025 年各注册分类预防用生物制品临床试验申请、NDA 批准/审评通过情况详见表10,2021 年至2025 年各注册分类预防用生物制品临床试验申请批准情况详见图33,2021 年至2025 年各注册分类预防用生物制品NDA审评通过情况详见图34。
表10 2025 年各注册分类预防用生物制品临床试验申请、NDA 批准/审评通过情况
|
注册申请类别 |
注册分类 |
预防用生物制品 |
||
|
注册申请(件) |
品种(个) |
|||
|
临床试验申请 |
创新型疫苗 |
1.1 |
4 |
4 |
|
1.2 |
27 |
17 |
||
|
1.3 |
14 |
9 |
||
|
1.4 |
12 |
10 |
||
|
改良型疫苗 |
2.2 |
7 |
5 |
|
|
2.5 |
2 |
1 |
||
|
2.6 |
1 |
1 |
||
|
境内或境外已上市疫苗 |
3.1 |
4 |
4 |
|
|
3.2 |
3 |
3 |
||
|
3.3 |
13 |
7 |
||
|
合计 |
87 |
61 |
||
|
NDA |
创新型疫苗 |
1.4 |
1 |
1 |
|
改良型疫苗 |
2.2 |
3 |
2 |
|
|
境内或境外已上市疫苗 |
3.1 |
3 |
2 |
|
|
3.2 |
1 |
1 |
||
|
3.3 |
9 |
6 |
||
|
合计 |
17 |
12 |
||
|
总计 |
104 |
73 |
||


(2)治疗用生物制品
批准治疗用生物制品临床试验申请 1220件,以注册分类统计,包括创新治疗用生物制品临床试验申请 967件(637个品种),改良型治疗用生物制品临床试验申请188 件(75 个品种),境内或境外已上市治疗用生物制临床试验申请65 件(44 个品种)。
审评通过治疗用生物制品NDA202件,以注册分类统计,包括创新治疗用生物制品NDA 46 件(27 个品种),改良型治疗用生物制品NDA76 件(34 个品种),境内或境外已上市治疗用生物制品NDA80 件(45 个品种),其中包括生物类似药(3.3类)12 件(8 个品种)。
2025 年各注册分类治疗用生物制品临床试验申请、NDA 批准/审评通过情况详见表11,2021 年至2025 年各注册分类治疗用生物制品临床试验申请批准情况详见图35,2021 年至2025 年各注册分类治疗用生物制品NDA审评通过情况详见图36。
表11 2025 年各注册分类治疗用生物制品临床试验申请、NDA 批准/审评通过情况
|
注册申请类别 |
注册分 类 |
治疗用生物制品 |
||
|
注册申请(件) |
品种(个) |
|||
|
临床试验申请 |
创新型生物制品 |
1 |
967 |
637 |
|
改良型生物制品 |
2.1 |
14 |
10 |
|
|
2.1;2.2 |
6 |
3 |
||
|
2.2 |
158 |
55 |
||
|
2.2;2.4 |
1 |
1 |
||
|
2.4 |
9 |
6 |
||
|
境内或境外已上市生物制品 |
3.1 |
9 |
8 |
|
|
3.2 |
10 |
7 |
||
|
3.3 |
37 |
23 |
||
|
3.4 |
9 |
6 |
||
|
合计 |
1220 |
756 |
||
|
NDA |
创新型生物制品 |
1 |
46 |
27 |
|
改良型生物制品 |
2.1 |
7 |
2 |
|
|
2.1;2.2 |
2 |
1 |
||
|
2.2 |
67 |
31 |
||
|
境内或境外已上市生物制品 |
3.1 |
54 |
26 |
|
|
3.2 |
7 |
4 |
||
|
3.3 |
12 |
8 |
||
|
3.4 |
7 |
7 |
||
|
合计 |
202 |
106 |
||
|
总计 |
1422 |
862 |
||


批准的治疗用生物制品临床试验申请 1220件中,抗肿瘤药物占比59.51%,皮肤及五官科药物占比6.97%,风湿性疾病及免疫药物占比5.08%。2025 年批准治疗用生物制品临床试验申请的适应症领域分布情况详见图37。

审评通过的治疗用生物制品 NDA202 件中,抗肿瘤药物占比42.08%,内分泌系统疾病药物占比15.84%,循环系统疾病药物6.93%。2025 年审评通过治疗用生物制品NDA 的适应症领域分布情况详见图38。

(三)直接行政审批类注册申请审结情况
2025 年审结直接行政审批类注册申请2271 件,其中无需技术审评的补充申请1885 件,临时进口注册申请386 件。2021 年至2025 年直接行政审批的各类别注册申请审结情况详见图39。

第三章药品加快上市注册情况
2025 年药审中心通过药品加快上市注册程序,加强与申请人的沟通交流,缩短药物研发与技术审评时间,加快临床急需新药好药上市。
(一)突破性治疗药物程序
药物临床试验期间,用于防治严重危及生命或者严重影响生存质量的疾病且尚无有效防治手段或者与现有治疗手段相比有足够证据表明具有明显临床优势的创新药或者改良型新药等,申请人可以在Ⅰ、聂期临床试验阶段,通常不晚于Ⅲ期临床试验开展前申请适用突破性治疗药物程序。药审中心对纳入突破性治疗药物程序的药物优先配置资源进行沟通交流,加强指导并促进药物研发。申请人在药物临床试验期间提出的沟通交流包括首次沟通交流、因重大安全性问题/重大技术问题而召开的会议、药物临床试验关键阶段会议以及一般性技术问题咨询等,药审中心予以优先处理。
2025年共收到突破性治疗药物程序申请424件,同意纳入突破性治疗药物程序101 件(89 项适应症,见附件 6),占申请数量的23.82%,较2024 年增加10.99%。
自2020年《药品注册管理办法》(总局第27号令)实施以来,累计纳入突破性治疗药物程序 395件(335项适应症),排名前三的分别为抗肿瘤药物、抗感染药物及神经系统疾病药物,具体适应症分布情况请见图41。


(二)附条件批准程序
药物临床试验期间,治疗严重危及生命且尚无有效治疗手段的疾病以及公共卫生方面急需的药品,药物临床试验已有数据显示疗效并能预测其临床价值的,以及应对重大突发公共卫生事件急需的疫苗或者国家卫生健康委认定急需的其他疫苗,经评估获益大于风险的,可基于替代终点、中间临床终点或早期临床试验数据而附条件批准上市。附条件批准上市的目的是缩短药物临床试验的研发时间,使其尽早应用于无法继续等待的危重疾病或公共卫生方面急需的患者。
2025年共有 38件药品注册申请(24项适应症)附条件批准上市,其中21项适应症为首次批准上市,3项适应症为已上市药品增加适应症(见附件7)。同时,在2025 年,共有13 项附条件批准的适应症完成确证性研究,转为常规批准。
2020 年《药品注册管理办法》(总局第27号令)实施以来,共有226件药品注册申请(160项适应症)附条件批准上市,包括抗肿瘤药物、新冠疫苗及治疗药物、血液系统疾病药物等,其中抗肿瘤药物数量最多,占比81.88%,共有42 项附条件批准的适应症完成确证性临床研究,转为常规批准,具体请见图42、图43。


(三)优先审评审批程序
药品上市许可申请时,对于以下具有明显临床价值的药品,可以申请适用优先审评审批程序:(一)临床急需的短缺药品、防治重大传染病和罕见病等疾病的创新药和改良型新药;(二)符合儿童生理特征的儿童用药品新品种、剂型和规格;(三)疾病预防、控制急需的疫苗和创新疫苗;(四)纳入突破性治疗药物程序的药品;(五)符合附条件批准的药品;(六)国家药监局规定其他优先审评审批的情形。适用优先审评审批程序的上市注册申请的审评时限由常规程序的200日缩短为130日,其中临床急需境外已上市罕见病用药的审评时限为70日。
2025 年共纳入优先审评审批注册申请133 件(92 个品种),同比增加7.26%,具体纳入情况见图44;2025年按照优先审评审批程序批准 124件注册申请(82个品种,其中4个品种新准上市后,同年又批准新适应症)上市,同比增加12.73%。

自2020年《药品注册管理办法》(总局第27号令)实施以来,共有629件药品注册申请纳入优先审评审批程序,包括抗肿瘤药物、皮肤及五官科药物、内分泌系统疾病药物等,其中抗肿瘤药物数量最多,占比41.97%,具体请见图45。

第四章药物研发与技术审评沟通交流
(一)沟通交流会议申请与办理情况
沟通交流是在药物研发与注册申请技术审评过程中,申请人与药审中心就关键技术问题等所进行的沟通交流。2025 年药审中心共接收沟通交流会议申请 5181件,办理沟通交流会议申请 4705件,为1783 家企业的4049 个品种(按照申请人提交沟通交流申请时的药品名称计,下同)提供了沟通交流服务,其中召开面对面会议/电话会议824 个,同比增加19.25%。2021 年至2025 年接收及办理沟通交流会议申请情况详见图46。
2025 年,药审中心办理沟通交流会议申请4705 件,在药物研发关键阶段办理的聂类会议占比 55.35%,其中新药临床试验申请前(Pre-IND)沟通交流会议申请占比19.04%,新药上市许可申请前(Pre-NDA)沟通交流会议申请占比 10.33%。2025年沟通交流会议申请接收及办理情况详见表12。

表12 2025 年沟通交流会议申请接收及办理情况(件)
|
沟通交流会议申请类型 |
接收量 |
接收占比 |
办理量 |
办理占比 |
|
|
Ⅰ类会议 |
703 |
13.57% |
596 |
12.67% |
|
|
Ⅱ类会议 |
新药临床试验申请前 (Pre-IND) |
952 |
18.37% |
896 |
19.04% |
|
新药临床试验申请(IND) |
89 |
1.72% |
94 |
2.00% |
|
|
完成Ⅰ期临床后(EndofphaseⅠ) |
350 |
6.76% |
302 |
6.42% |
|
|
完成Ⅱ期临床后(End ofphase Ⅱ) |
879 |
16.97% |
727 |
15.45% |
|
|
新药上市许可申请前 (Pre-NDA) |
515 |
9.94% |
486 |
10.33% |
|
|
新药上市许可申请(NDA) |
63 |
1.22% |
61 |
1.30% |
|
|
其他 |
177 |
3.42% |
38 |
0.81% |
|
|
Ⅲ类会议 |
1453 |
28.04% |
1505 |
31.99% |
|
|
总计 |
5181 |
100.00% |
4705 |
100.00% |
|
(二)一般性技术问题咨询情况
2025 年接收一般性技术问题咨询13202 个,为3505 家企业解答一般性技术问题咨询13022 个,及时总结梳理共性问题,并在中心网站予以发布,2025年按程序发布 15批共29个常见一般性技术问题解答,涵盖了注册受理、技术审评等方面,累计发布269 个共性问题1, 2021年至2025年接收及办理一般性技术问题咨询量详见图47。

1 见链接:https://www.cde.org.cn/main/xxgk/listpage/07edef25f1e7354bfd8490baa0ce056b
第五章完善药品技术指导原则体系
(一)制定发布药品技术指导原则
2025 年,药审中心继续加强药品技术评价体系建设,全年共发布技术指导原则49 项,累计发布指导原则超过600 项。
1.聚焦国际前沿技术领域,持续完善新兴产品、复杂药物的评价体系与技术指南聚焦创新型基因治疗药物、多肽药物、抗体药物、重组蛋白药物等新产品、新技术,制定发布《地中海贫血基因治疗产品临床试验技术指导原则(试行)》《重组腺相关病毒载体类体内基因治疗产品申报上市药学共性问题与技术要求》《肽类药物临床药理学研究技术指导原则》《抗体偶联药物临床药理学研究技术指导原则》《抗体类药物临床药理学研究技术指导原则》《重组糖蛋白激素类产品药学研究与评价技术指导原则》《重组胰高血糖素样肽-1受体激动剂药学研究与评价技术指导原则(试行)》,持续构建全生命周期的技术指南体系。
围绕疫苗研发与评价的关键环节,制定发布《疫苗临床试验不良事件分级标准指导原则(修订版)》《多联疫苗临床试验技术指导原则》《带状疱疹疫苗临床试验技术指导原则》《疫苗佐剂非临床研究技术指导原则》《疫苗临床试验技术指导原则》《疫苗说明书临床相关信息撰写指导原则(试行)》《预防用 mRNA疫苗非临床研究技术指导原则》等,持续完善覆盖疫苗药学、非临床和临床的综合评价体系与技术指南。为积极防控公共卫生事件,及时发布猴痘疫苗及药品的技术要求,制定了《预防用猴痘疫苗药学研究技术指导原则(试行)》《预防用猴痘疫苗非临床有效性研究技术指导原则(试行)》《抗猴痘病毒药物临床试验技术指导原则(试行)》。
完善放射性药物的审评标准体系,制定《放射性治疗药物申报上市临床风险管理计划技术指导原则》,更好地为放射性药物临床研发提供指导和服务。
针对生物类似药,制定了《生物类似药药学相似性研究的问题与解答》《生物类似药说明书撰写技术指导原则》。
2.聚焦重大疾病领域的临床关键问题,立足临床需求,健全创新药物临床评价体系
在重大慢病方面,制定发布《骨关节炎新药临床研发技术指导原则》《患者报告结局指标用于风湿免疫性疾病临床试验的技术指导原则》《晚期胃癌新药临床试验设计指导原则》《治疗子宫内膜癌新药临床研发技术指导原则(试行)》《单臂临床试验用于支持抗肿瘤药物常规上市申请技术指导原则》《治疗慢性气道疾病的靶向炎症因子类生物制剂临床试验技术指导原则(试行)》《针对泛肿瘤的抗肿瘤药物临床研发技术指导原则》《阿尔茨海默病治疗药物临床试验技术指导原则(试行)》。
在重大感染性疾病方面,制定发布《存在未满足临床需求的严重细菌感染性疾病抗菌药物临床试验技术指导原则》《抗HIV感染药物临床耐药性研究及数据递交指导原则》《艾滋病免疫功能重建不全治疗药物临床试验技术指导原则》。
3.围绕特殊人群用药需求提升临床研究质量
在以患者为中心的研发理念指导下,基于儿童和老年患者用药需求及人群特征,制定发布《儿童药物临床试验安全信息评估与报告技术指导原则(试行)》《创新药研发中涉及适老化设计时的一般原则及考虑要点(试行)》《老年人群参与创新药临床试验的关键要素及试验设计要点(试行)》《药品说明书中涉及老年人群用药信息的撰写要点(试行)》。
为解决罕见疾病药物研发面临的现实困难和重要问题,制定发布《嗜酸性粒细胞性食管炎治疗药物临床试验技术指导原则》《罕见疾病药物临床药理学研究技术指导原则》《模型引导的罕见疾病药物研发技术指导原则》,为罕见疾病药物研发提供独特的研发策略、技术手段以及有效的数据分析工具。
4.总结仿制药研发关键技术问题,推动仿制药研发高质量发展
围绕仿制药研发中的关键技术问题,制定发布《局部起效化学仿制药体外释放(IVRT)与体外透皮(IVPT)研究技术指导原则(试行)》《发酵或半合成化学仿制药抗生素有关物质限度制定指导原则》《化学仿制药口服制剂经肠内营养管给药体外对比研究技术指导原则》,提升仿制药研发的科学性和规范性,推动产业高质量发展。
5.关注药品研发多专业领域技术要求,助力新药研发提质加速
在药学研究方面,发布了《化学药品口溶膜剂药学研究技术指导原则(试行)》《化药口服固体制剂中间产品存放时限研究技术指导原则》。在药学变更方面,发布了《化学药品批准后药学变更管理方案技术指导原则(试行)》《已上市血液制品生产场地变更研究技术指导原则(试行)》,进一步夯实药品质量控制与变更管理的科学依据。
在创新药临床技术要求方面,发布了《口服药物胃pH 依赖性药物相互作用评价技术指导原则》《药物暴露-效应关系研究技术指导原则》《创新药研发期间风险管理计划撰写技术指导原则(试行)》,进一步完善临床和临床药理学评价体系,为新药剂量探索、相互作用评价提供方法学支持,为新药风险管理计划提供技术指导。
为加快建立和完善符合中药特点的技术评价体系,促进基于人用经验的中药复方制剂新药的研发注册,制定了《中药复方制剂新药研发人用经验收集整理技术指导原则(试行)》。
(二)推动ICH指导原则转化实施
1.国家药监局成功当选ICH 监管活动医学词典(MedDRA)指导委员会成员
2025年5月ICH马德里会议上,经ICH管理委员会投票推选,国家药监局成功当选ICHMedDRA指导委员会成员,任期3年。这是MedDRA 指导委员会自2025 年改组以来首次扩增成员。成功当选意味着国家药监局将更进一步深度参与国际规则制定和 ICH 管理工作。
2.紧跟技术前沿,全面参与ICH议题国际协调
2025年,国家药监局共累计选派83人参与48个ICH 议题工作组的国际协调,参加643场电话会议,持续深入参与ICH指导原则的制修订,及时分享我国相关药品监管实践经验,并积极吸纳借鉴全球新理念、新方法、新工具和新标准。
3.着力推进药品注册技术要求与国际接轨
2025 年,国家药监局采纳《M14:使用真实世界数据进行药品安全性评估的非干预性研究:规划、设计、分析和报告的一般原则》和《M11:临床电子结构化协调方案》2 个新制定的ICH 指导原则,采纳《E6(R3):药物临床试验质量管理规范技术指导原则》和《E2D(R1):上市后安全数据:个例安全性报告管理和报告的定义和标准》2 个新修订的指导原则,并开始实施《Q5A(R2):来源于人或动物细胞系生物技术产品的病毒安全性评价》和《Q4B:药典》2个指导原则。截至2025 年12月31 日,国家药监局已采纳实施73 个ICH 指导原则。
药审中心在参与 ICH 议题协调和实施的全过程中,始终高度关注行业、学界代表对国内实施ICH 指导原则的相关意见建议,积极加强与国内外行业协会及工业界的交流合作,全年累计召开国内专家研讨会 15场;此外,通过药审云课堂、药审技术讲堂、直播培训等形式开展宣贯培训6 场,提升了国内实施和遵循水平。
第六章药品监管科学研究
药审中心聚焦国际药品监管前沿技术,结合国家科技发展战略要求,依托国家重点研发计划、国家药监局“中国药品监管科学行动计划”、国家卫生健康委重点专项、中医药现代化专项、药品监管科学全国重点实验室、广州国家实验室专项等平台,组织实施了65项药品监管科学研究,过程中与117 家产学研监等相关方持续互动交流,团结优势科研立项,开展了26次公开宣讲,发表了49 篇学术论文,固化形成新的监管理念、工具和方法以及药品研发与评价技术标准,形成22 项技术指导原则,21 项调研报告,并将其引入药品审评过程,推动新技术转化应用和产业高质量发展、更好地满足公众用药需求。
(一)完善细胞与基因治疗药品的技术评价标准体系
药审中心通过开展细胞与基因治疗药品的技术审评标准体系研究,制定了《细胞治疗药品药学变更研究与评价技术指导原则》等9 项技术指导原则,进一步完善技术审评体系。通过多层次的沟通交流,促进企业研发和申报细胞与基因治疗药品的规范性,提高了研发和申报效率,推动药品上市应用进程。截至2025 年12月31 日,已支持推动8 款CAR-T细胞治疗药品在国内上市,用于治疗复发难治性淋巴瘤、白血病、多发性骨髓瘤等疾病,国内首款干细胞治疗药品上市用于移植物抗宿主病,国内首款基因治疗药物上市用于治疗血友病,为相关领域患者提供了新的治疗选择。
药审中心相关工作组在监管科学研究取得的成果基础上,积极参与ICH细胞和基因治疗讨论组(CGTDG)沟通讨论,充分表达我国已经制定发布的相关技术指南和监管框架,为CGTDG 工作组熟悉我国监管相关技术要求,确定细胞与基因治疗药品临床方面协调的优先议题发挥了积极作用。
(二)完善创新疫苗技术评价标准体系
药审中心牵头开展了“人用疫苗新型佐剂的技术评价研究”课题,2025年度发布了《疫苗佐剂非临床研究技术指导原则》,起草了《预防用疫苗佐剂药学研究技术指导原则(试行)》,首次制定了佐剂药学技术指南,完善了佐剂疫苗技术评价体系,助力多款含新型佐剂的IND 疫苗品种获批。疫苗类型涵盖流感疫苗、呼吸道合胞疫苗、带疱疫苗、狂犬疫苗、结核疫苗等。在含新型佐剂疫苗审评数量以及佐剂研发种类推进方面,均较以往明显增加。
结合产业化过程中实际出现的问题、新技术不断引进等情况,药审中心将 ICH 等研发理念、先进的分析方法及工具引入多糖结合疫苗全生命周期,通过工艺表征、全过程控制、全面的产品结构解析及引入先进分析方法等,建立此类产品药学研究及评价的体系,鼓励、规范和指导多糖结合疫苗的研发水平全面提升,制定了《多糖结合疫苗药学研究及评价技术指导原则(试行)》,为全球首个多糖结合疫苗药学开发全过程的通用型指南,有效填补了国内外空白;完成了《多糖结合疫苗核磁共振研究的技术考虑(征求意见稿)》,为全球首个指导多糖、多糖结合物等大分子核磁共振技术研究的指南,有助于解决工艺放大、质量提升等行业集中问题,促进计划免疫产品更新换代。课题开展期间,共推动20个多糖结合疫苗进入临床,包含国内首个B 族链球菌结合疫苗、ACYW135X 群脑膜炎球菌多糖结合疫苗,多个高价次的肺炎球菌多糖结合疫苗等,有效的弥补产业空白,提升技术储备和创新能力;推动5个国产品种进入上市申报阶段,为多糖结合疫苗创新发展提供了技术支撑,推动了多糖结合疫苗技术标准升级及产业链升级。
(三)进一步建立符合中医药特点的中药审评证据体系
药审中心进一步建立健全符合中医药特点的中药安全、疗效评价方法和技术标准,加快构建中医药理论、人用经验和临床试验相结合的中药注册审评证据体系(简称“三结合”体系),促进已上市中药二次开发。作为支持中药注册上市证据的人用经验,如何进行收集整理及中药改良型新药,如何基于“三结合”理念促进中药二次开发的技术要求亟待研究明确。药审中心以临床价值为导向,通过调查研究、座谈、专题研讨、征求意见等方式,结合实践细化了人用经验收集整理与中药改良型新药研发的具体技术要求。研究成果现已转化到《中药复方制剂新药研发人用经验收集整理技术指导原则(试行)》当中,且《中药改良型新药研究技术指导原则(试行)》已发布。药审中心通过召开专题研讨会、实地调研、对外宣贯培训等近30场,增强了行业专家和新药研发者的信心和产业活力。课题在研期间,每年获批中药新药10个以上,16个古代经典名方中药新药,2个中药改良型新药,10 余个品种基于中医药理论、人用经验无需开展药效学试验,2 个中药复方制剂基于中医药理论、人用经验直接开展确证性临床试验,涉及呼吸、消化、内分泌等多个中医优势病种。药审中心运用以上研究成果,通过沟通交流指导多个品种精准申报和开展研发,通过技术标准的制定进一步促进了名老中医方、医疗机构中药制剂等向中药新药转化,为已上市中药二次开发提供指导。
(四)推进新方法学(NAMs)的监管标准制定
药审中心和中检院联合涵盖产、学、研领域的7家机构共同推进部分类器官/器官芯片方法学的验证和探索适用的应用场景,下一步计划在监管端、技术研发端与产业应用端多方协作的机制下,通过开展类器官/器官芯片更加细化、规范的多中心联合验证及第三方测试验证,提高方法标准化水平以及预测准确性及可靠性,推动类器官与器官芯片新技术验证应用标准及监管接受框架的建立。
第七章药品研发与技术审评宣贯与培训
(一)深入开展药审云课堂
药审中心打造药审云课堂课程体系,在持续加强创新药研发、前沿技术领域与国际监管共识等宣讲的同时,及时总结和回顾申请人普遍关注的共性问题,结合典型案例进行集中解答与分享。不断创新药审云课堂互动形式,注重听取业界意见建议,打造“线上线下”相结合的培训互动形式,2025 年共举办12 期,开展授课56 讲,共计13万余人在线观看,药审云课堂参与机构分布见图48。

1.以问题为导向设计课程,鼓励医药产业创新
2025 年药审云课堂围绕审评业务管理、新药临床研发技术考虑、中药、化学药及生物制品审评常见共性问题三方面布局课程体系。审评业务管理方面持续解析一般性技术问题咨询、电子申报及申报常见问题等内容,尤其对申请人高质量开展沟通交流推出了一系列课程;
新药临床研发课程体系从临床、临床药理、非临床各环节进行了深入解读,并对II 期进III期沟通交流要点等关键技术问题进行专题讲解;另外总结中药、化学药品及生物制品不同产品在审评过程中的常见共性问题,增加实际案例帮助申请人更好理解和把握技术要求的深层含义,其中化学药品方面,侧重对自评估报告、原料药及制度工艺信息表核定要求等进行讲解;中药方面,侧重对注册受理、沟通交流会议资料准备、已上市中药变更及中药说明书撰写等进行分享;生物制品方面,侧重对注册受理、细胞与基因治疗药品技术要求解读等进行交流;另外对申请人普遍关注的药品注册核查检验专题也进行了相应讲解。
2.结合国家药监局部署及中心重点工作进行专题宣讲
结合中心重点工作,2025 年度药审云课堂重点从助力补充申请试点、推动仿制药高质量研发、鼓励临床急需新药好药研发三方面开展了专题解读。其中在补充申请试点工作方面,以“变更”为主线,分期开展了临床期间变更和已上市变更技术要求等课程;为推动高质量仿制药研发,系统梳理了仿制药受理常见问题、申报资料要求撰写、一般性技术问题咨询、生物等效性研究、工艺研究、补充申请等常见问题解析课程;及时解读新发布药品技术指导原则,重点解读了抗肿瘤药物和罕见病治疗药物研发相关的监管考虑等。
3.开展线上线上相结合药审云课堂,丰富互动方式
为提高药审云课堂的互动性,打破线上直播提问互动的局限性,2025 年药审中心分别联合药品长三角分中心、药品大湾区分中心、京津冀分中心、西南分中心举办了4场“线上+线下”相结合的药审云课堂,带领药审云课堂“走出去”,不仅在培训期间面向全国直播和答疑,同时对于线下参与的申请人能够进行面对面的交流和指导,进一步提高药审云课堂的宣贯效能。
4.打造药审云课堂平台,持续完善课程体系
积极响应业界需求,打造药审云课堂平台和观看友好的课程界面,方便申请人随时观看回放,累计上传164 个课程视频,目前中心网站“药审云课堂”平台已形成了覆盖各专业领域的课程体系,从沟通交流、受理、审评全流程的基础性讲解,到申请人较为关注的沟通要点、申报资料撰写、审评中关键技术问题(如变更、药学研究、临床研究等)等主题均有较为全面的课程,满足业界研发注册的基本需求。
(二)开展服务区域发展药品注册技术培训班
在药审云课堂基础上,药审中心分别赴河北、江西、湖北、陕西等地开展药品注册技术系列培训班4场,近3000余人参训。内容覆盖中药、化学药品、生物制品药物研发共性问题与申报常见问题交流,ICH 技术要求解读、疫苗、细胞与基因治疗药品技术要求、中药质量控制及“三结合”注册审评证据体系下中药新药研发监管考虑、改良型新药监管考虑等。针对性解决区域内企业药品研发中存在的痛点难点问题,加快产品研发申报进程,助力区域医药产业高质量发展。
第八章2025 年度药品审评主要工作回顾
(一)2025 年1月21 日,国家药监局发布《关于简化港澳已上市传统口服中成药内地上市注册审批的公告》(2025年第 7号),决定对港澳已上市传统口服中成药在内地上市注册实施简化审批,进一步支持香港特别行政区、澳门特别行政区中医药事业发展。4月18日,药审中心发布《简化港澳已上市传统口服中成药内地上市注册审批申报资料及技术要求》,明确了简化注册审批的资料及技术要求。5 月19日,药审中心发布《关于港澳已上市传统口服中成药内地上市注册沟通交流服务有关事宜的通知》,规定港澳已上市传统口服中成药内地上市许可申请递交前,申请人可根据需要提出沟通交流或咨询。
(二)2025 年1月23 日,国家药监局发布《关于扩大药品电子通用技术文档实施范围的公告》(2025 年第10号),规定自2025 年1月27 日起,化学药品 1类至5类的药物临床试验申请,化学药品2类、3类、4类、5.2类的上市许可申请,以及预防用生物制品和治疗用生物制品1类至3类的药物临床试验申请、2类和3类的上市许可申请,可按照eCTD 进行申报,加快推进了eCTD 在我国的实施进程。
(三)2025年 3 月 25日,国家药监局、国家卫生健康委颁布2025 年版《中华人民共和国药典》,自2025 年10月1 日起施行。
(四)2025年5月11 日至12 日,ICH2025年线下会议在西班牙马德里召开,国家药监局当选为ICH监管活动医学词典(MedDRA)指导委员会成员。
2 2025 年药审中心发布的指导原则和开展的培训见附件8、附件9,未列入主要工作回顾。
(五)2025 年5月29 日,药审中心发布儿童抗肿瘤药物研发鼓励试点计划(星光计划),加强与申请人的沟通交流,就抗肿瘤药物儿童人群研究过程中技术难点向申请人提供针对性指导,提高儿童抗肿瘤药物的研发效率。
(六)2025 年8月28 日,药审中心发布《化学药品仿制药上市许可申请模块二药学资料撰写要求(试行)》,规定自2026年3月 1日起,化学药品仿制药上市许可申请(包括化学药品3类、4类、5.2类和原料药)申报资料需按照该撰写要求提交,从而提高仿制药申报资料质量,促进仿制药质量提升。
(七)2025 年9月12 日,国家药监局发布《关于优化创新药临床试验审评审批有关事项的公告》(2025 年第86号),对获国家全链条支持创新药发展政策体系支持的具有明显临床价值的重点创新药品种、审评中心公布的符合条件的儿童创新药、罕见病创新药,以及中药创新药品种、全球同步研发品种的临床试验申请,在受理后 30个工作日内完成审评审批,进一步支持以临床价值为导向的创新药研发,提高临床研发质效。药审中心同步发布创新药临床试验申请申报资料要求等相关文件,明确了此类临床试验申请的具体资料要求。截至12月31日,已受理30日通道临床试验申请55 件,完成审评审批20件。
(八)2025年9月21 日至24 日,国家药监局分别在北京市、湖北省武汉市、重庆市举行药品和医疗器械审评检查京津冀分中心、华中分中心、西南分中心挂牌仪式。
(九)2025 年9月30 日,国家药监局发布《关于境外已上市药品获批前商业规模批次产品进口有关事宜的公告》(2025 年第96号),规定境外已上市药品在我国获批上市后,对符合要求的获批前商业规模批次产品,允许进口并上市销售,支持创新药品和急需药品尽早用于临床、惠及患者。
(十)2025年12月24 日,国家药监局发布关于适用《E6(R3):药物临床试验质量管理规范技术指导原则》国际人用药品注册技术协调会指导原则的公告,规定自2026 年3月31 日后实施的药物临床试验,均适用E6(R3)指导原则。
(十一)2025年,国家药监局批复同意辽宁、安徽、江西、陕西、吉林、海南省药监局开展优化药品补充申请审评审批程序改革试点,累计已有十六个省(市)药监局开展药品补充申请审评审批程序改革试点,为辖区内药品重大变更申报前提供前置指导、核查、检验和立卷服务。
(十二)2025 年,国家药监局批准创新药76 个,其中新机制新靶点药物11 个,均创历史新高。
结语
2026 年是“十五五”规划开局之年,药审中心将在国家药监局党组坚强领导下,深入学习贯彻党的二十大和二十届历次全会精神,认真落实国家药监局党组部署要求,按照“讲政治、强监管、保安全、促发展、惠民生”的工作思路,统筹推进全年重点工作。全力推进全面深化药品监管改革各项任务,着力推动药品试验数据保护制度落地实施,落实对重点品种实行“提前介入、一企一策、全程指导、研审联动”要求,稳步开展仿制药上市申请前置服务改革试点,持续提升药品申报质量和审评审批质效;围绕全面加强药品监管能力建设,持续完善与药品审评检查分中心协同联动机制,深化多渠道多层次沟通交流,推进eCTD 全面实施,探索人工智能辅助审评,深入开展药品监管科学研究,持续推动药品审评技术要求与ICH 规则协调一致。药审中心将继续坚持以人民健康为中心,切实保障药品高水平安全,促进医药产业高质量发展,更好满足人民群众用药需求,为推进健康中国建设贡献药审力量。
附件1 2025 年国家药监局批准的创新药
2025 年国家药监局批准的创新药
|
序号 |
药品名称 |
上市许可持有人 |
药品类型 |
治疗领域 |
适应症/功能主治 |
加快上市程序 |
|
1 |
阿夫凯泰片 |
Cytokinetics, Incorporated |
化学药品 |
循环系统疾病药物 |
本品用于治疗纽约心脏协会(NYHA)心功能分级II-III级的梗阻性肥厚型心肌病(HCM)成人患者,以改善运动能力和症状。 |
突破性治疗优先审评审批 |
|
2 |
艾考磷布韦片 |
宜昌东阳光长江 药业股份有限公 司 |
化学药品 |
抗感染药物 |
本品与磷酸萘坦司韦胶囊联用,治疗初治或干扰素经治的基因1、2、3、6型成人慢性丙型肝炎病毒(HCV)感 染,可合并或不合并代偿性肝硬化。 |
|
|
3 |
安瑞克芬注射液 |
海思科医药集团 股份有限公司 |
化学药品 |
镇痛药及麻醉科用药 |
本品适用于治疗腹部手术后的轻、中度疼痛。 |
|
|
本品用于维持性血液透析的慢性肾脏疾病相关中重度瘙痒成人患者。 |
优先审评审批 |
|||||
|
4 |
昂拉地韦片 |
广东众生睿创生物科技有限公司 |
化学药品 |
抗感染药物 |
用于成人单纯型甲型流感患者的治疗,不包括存在流感相关并发症高风险的患者。 |
|
|
5 |
奥格特韦钠胶囊 |
浙江艾森药业有限公司 |
化学药品 |
抗感染药物 |
本品用于治疗轻中型新型冠状病毒感染(COVID-19)的成年患者。 |
附条件批准 |
|
6 |
吡洛西利片 |
轩竹生物科技股份有限公司 |
化学药品 |
抗肿瘤药物 |
本品联合氟维司群,适用于既往接受内分泌治疗后出现疾病进展的激素受体(HR)阳性、人表皮生长因子受体 2 (HER2)阴性晚期或转移性乳腺癌成人患者。 |
|
|
单药用于既往转移性阶段接受过两种及以上内分泌治疗和一种化疗后出现疾病进展的激素受体(HR)阳性、人表皮生长因子受体 2(HER2)阴性晚期或转移性乳腺癌成人患者。 |
|
7 |
氘恩扎鲁胺软胶囊 |
海创药业股份有限公司 |
化学药品 |
抗肿瘤药物 |
本品适用于接受醋酸阿比特龙及化疗后出现疾病进展,且既往未接受新型雄激素受体抑制剂的转移性去势抵抗性前列腺癌(mCRPC)成人患者。 |
|
|
8 |
地罗阿克片 |
轩竹生物科技股份有限公司 |
化学药品 |
抗肿瘤药物 |
本品单药适用于未经过间变性淋巴瘤激酶(ALK)抑制剂治疗的ALK 阳性的局部晚期或转移性非小细胞肺癌 (NSCLC)患者的治疗。 |
|
|
9 |
芬妥司兰纳注射液 |
Genzyme Corporation |
化学药品 |
血液系统疾病药物 |
本品适用于患有以下疾病的12 岁及以上儿童和成人患者的常规预防治疗,以防止出血或降低出血发作的频率: 存在或不存在凝血因子VIII 抑制物的重型A型血友病 (先天性凝血因子VIII 缺乏,FVIII<1%)或存在或不存在凝血因子IX 抑制物的重型B型血友病(先天性凝血因子IX缺乏,FIX<1%)。 |
|
|
10 |
枸橼酸伏维西利胶囊 |
锦州奥鸿药业有限责任公司 |
化学药品 |
抗肿瘤药物 |
本品联合氟维司群,适用于既往接受内分泌治疗后出现疾病进展的激素受体(HR)阳性、人表皮生长因子2 (HER2)阴性的复发或转移性成年乳腺癌患者。 |
|
|
本品适用于激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性局部晚期或转移性乳腺癌成人患者:与芳香化酶抑制剂联合使用作为初始内分泌治疗。 |
||||||
|
11 |
枸橼酸戈来雷塞片 |
上海艾力斯医药 科技股份有限公 司 |
化学药品 |
抗肿瘤药物 |
本品适用于至少接受过一种系统性治疗的鼠类肉瘤病毒癌基因(KRAS)G12C 突变型的晚期非小细胞肺癌 (NSCLC)成人患者。 |
突破性治疗附条件批准优先审评审批 |
|
12 |
酒石酸泰瑞西利胶囊 |
贝达药业股份有限公司 |
化学药品 |
抗肿瘤药物 |
本品联合氟维司群,适用于既往接受内分泌治疗后进展的激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性的局部晚期或转移性成年乳腺癌患者。 |
|
|
13 |
卡匹色替片 |
AstraZeneca UKLimited |
化学药品 |
抗肿瘤药物 |
本品联合氟维司群用于转移性阶段至少接受过一种内分泌治疗后疾病进展,或在辅助治疗期间或完成辅助治疗后 |
|
12 个月内复发的激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性且伴有一种或多种 PIK3CAAKT1PTEN改变的局部晚期或转移性乳腺癌成人患者。 |
||||||
|
14 |
库莫西利胶囊 |
正大天晴药业集团股份有限公司 |
化学药品 |
抗肿瘤药物 |
本品联合氟维司群,适用于既往接受内分泌治疗后出现疾病进展的激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性的局部晚期或转移性乳腺癌成人患者。 |
|
|
15 |
利厄替尼片 |
江苏奥赛康药业有限公司 |
化学药品 |
抗肿瘤药物 |
既往经EGFR 酪氨酸激酶抑制剂(TKI)治疗时或治疗后出现疾病进展,并且经检测确认存在EGFR T790M 突变阳性的局部晚期或转移性NSCLC 成人患者的治疗。 |
|
|
本品适用于具有表皮生长因子受体(EGFR)外显子19 缺失或外显子21(L858R)置换突变的局部晚期或复发转移性非小细胞肺癌(NSCLC)成人患者的一线治疗。 |
||||||
|
16 |
利沙托克拉片 |
苏州亚盛药业有限公司 |
化学药品 |
抗肿瘤药物 |
本品适用于既往经过至少包含布鲁顿酪氨酸激酶(BTK)抑制剂在内的一种系统治疗的成人慢性淋巴细胞白血病(CLL)小淋巴细胞淋巴瘤(SLL)患者 |
附条件批准优先审评审批 |
|
17 |
磷酸萘坦司韦胶囊 |
广东东阳光药业股份有限公司 |
化学药品 |
抗感染药物 |
本品与艾考磷布韦片联用,治疗初治或干扰素经治的基因1、2、3、6型成人慢性丙型肝炎病毒(HCV)感染,可合并或不合并代偿性肝硬化。 |
|
|
18 |
硫酸艾玛昔替尼片 |
江苏恒瑞医药股份有限公司 |
化学药品 |
风湿性疾病及免疫药物 |
本品适用于对一种或多种TNF 抑制剂疗效不佳或不耐受的活动性强直性脊柱炎成人患者。 |
|
|
本品适用于对一种或多种TNF 抑制剂疗效不佳或不耐受的中重度活动性类风湿关节炎成人患者。 |
||||||
|
本品用于对局部外用治疗或其他系统性治疗应答不充分或不耐受的中重度特应性皮炎成人患者。 |
|
本品适用于成人重度斑秃患者。 |
||||||
|
19 |
芦沃美替尼片 |
上海复星医药产业发展有限公司 |
化学药品 |
抗肿瘤药物 |
朗格汉斯细胞组织细胞增生症和组织细胞肿瘤:本品适用于朗格汉斯细胞组织细胞增生症(LCH)和组织细胞肿瘤成人患者。 |
突破性治疗优先审评审批 |
|
伴有症状、无法手术的丛状神经纤维瘤的I 型神经纤维瘤病:本品适用于2岁及2岁以上伴有症状、无法手术的丛状神经纤维瘤(PN)的 I型神经纤维瘤病(NF1)儿童及青少年患者。 |
优先审评审批 |
|||||
|
20 |
马来酸美凡厄替尼片 |
杭州中美华东制药有限公司 |
化学药品 |
抗肿瘤药物 |
本品适用于具有表皮生长因子受体(EGFR)外显子21(L858R)置换突变的局部晚期或转移性非小细胞肺癌 (NSCLC)成人患者的一线治疗。 |
|
|
21 |
玛帕西沙韦胶囊 |
康元药业集团股份有限公司 |
化学药品 |
抗感染药物 |
本品适用于既往健康的12 岁及以上青少年和成人单纯性甲型和乙型流感患者的治疗,不包括存在流感相关并发症高风险的患者。 |
|
|
22 |
玛仕度肽注射液 |
信达生物制药 (苏州)有限公 司 |
化学药品 |
内分泌系统疾病药物 |
本品适用于在控制饮食和增加体力活动基础上对成人患者的长期体重控制,初始体重指数(BMI)为: BMI≥28 kgm2(肥胖),或 BMI≥24 kgm2(超重),并伴有至少一种体重相关的合并症(例如高血糖、高血压、血脂异常、脂肪肝、阻塞性睡眠呼吸暂停综合征等)。 |
|
本品适用于成人2型糖尿病患者的血糖控制: 单药治疗 :单纯饮食控制和运动干预后血糖仍控制不佳的成人2型糖尿病患者; 联合治疗 :在饮食控制和运动基础上,接受二甲双胍和/或磺脲类药物、接受二甲双胍和/或钠-葡萄糖共转运蛋白2 抑制剂(SGLT2i)类药物治疗血糖仍控制不佳的成人2型糖尿病患者。 |
||||||
|
23 |
玛舒拉沙韦片 |
江西科睿药业有限公司 |
化学药品 |
抗感染药物 |
适用于既往健康的12 岁及以上青少年和成人单纯性甲型和乙型流感患者的治疗,不包括存在流感相关并发症高风险的患者。 |
|
|
24 |
玛硒洛沙韦片 |
南京征祥医药有限公司 |
化学药品 |
抗感染药物 |
用于既往健康的成人单纯性甲型和乙型流感患者的治疗,不包括存在流感相关并发症高风险的患者。 |
|
|
25 |
莫米司特片 |
赣州和美药业股份有限公司 |
化学药品 |
皮肤及五官科药物 |
本品适用于治疗符合接受光疗或系统治疗指征的中度至重度斑块状银屑病的成人患者。 |
优先审评审批 |
|
26 |
那米司特片 |
Boehringer Ingelheim International GmbH |
化学药品 |
呼吸系统疾 病及抗过敏药物 |
用于治疗特发性肺纤维化(IPF)成人患者。 |
优先审评审批 |
|
用于治疗进展性肺纤维化(PPF)成人患者。 |
优先审评审批 |
|||||
|
27 |
苹果酸法米替尼胶囊 |
江苏恒瑞医药股份有限公司 |
化学药品 |
抗肿瘤药物 |
本品联合注射用卡瑞利珠单抗用于既往接受含铂化疗治疗失败但未接受过贝伐珠单抗治疗的复发或转移性宫颈癌患者。 |
突破性治疗附条件批准 |
|
28 |
苹果酸司妥吉仑片 |
上海上药信谊药厂有限公司 |
化学药品 |
循环系统疾病药物 |
原发性高血压。 |
|
|
29 |
普卢格列汀片 |
石药集团欧意药业有限公司 |
化学药品 |
内分泌系统疾病药物 |
本品适用于改善成人2 型糖尿病患者的血糖控制。 单药治疗:本品单药可配合饮食控制和运动,用于改善成 |
|
人2 型糖尿病患者的血糖控制。 与盐酸二甲双胍联合治疗: 当单独使用盐酸二甲双胍仍不能有效控制血糖时,本品可与盐酸二甲双胍联合使用,在饮食和运动基础上改善成人2型糖尿病患者的血控制。 |
||||||
|
30 |
瑞格列汀二甲双胍片 (Ⅰ)/(聂) |
山东盛迪医药有限公司 |
化学药品 |
内分泌系统疾病药物 |
本品配合饮食控制和运动,适用于接受磷酸瑞格列汀盐二甲双胍治疗的 2型糖尿病成人患者改善血控制。 |
|
|
31 |
瑞美吡嗪注射液 |
杭州中美华东制药有限公司 |
化学药品 |
医学影像学药物 |
本品是一种注射用外源性荧光示踪剂,需与美德康公司(MediBeaconIne)生产的经皮肾小球滤过率测量设备 (TGFR)配合使用,评估患者的肾小球滤过率(GFR)。 |
|
|
32 |
瑞米布替尼片 |
NovartisPharma Schweiz AG |
化学药品 |
皮肤及五官科药物 |
本品适用于H1 抗组胺药控制不充分的成人慢性自发性荨麻疹患者。 |
优先审评审批 |
|
33 |
塞纳帕利胶囊 |
上海英派药业有限公司 |
化学药品 |
抗肿瘤药物 |
本品适用于晚期上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者在一线含铂化疗达到完全缓解或部分缓解后的维持治疗。 |
|
|
34 |
索托克拉片 |
百济神州(苏 州)生物科技有 限公司 |
化学药品 |
抗肿瘤药物 |
既往接受过至少包含布鲁顿酪氨酸激酶(BTK)抑制剂在内的一种系统治疗的慢性淋巴细胞白血病(CLL)小淋巴细胞淋巴瘤(SLL)成人患者 |
附条件批准优先审评审批 |
|
既往接受过至少两种系统性治疗(含布鲁顿酪氨酸激酶[BTK]抑制剂)的复发或难治性套细胞淋巴瘤(MCL)成人患者。 |
附条件批准优先审评审批 |
|||||
|
35 |
维培那肽注射液 |
派格生物医药(杭州)股份有 |
化学药品 |
内分泌系统疾病药物 |
本品适用于成人2型糖尿病患者的血糖控制: 单药治疗:单纯饮食控制和运动干预后血糖仍控制不佳的 |
|
限公司 |
成人2型糖尿病患者。 联合治疗:在饮食控制和运动基础上,接受二甲双胍治疗血糖仍控制不佳的成人2型糖尿病患者。 |
|||||
|
36 |
盐酸阿曲生坦片 |
NovartisPharma Schweiz AG |
化学药品 |
肾脏泌尿系统疾病药物 |
本品适用于降低有疾病快速进展风险的原发性免疫球蛋白A肾病(IgA肾病)成人患者的蛋白尿。一般来说,这类患者的尿蛋白肌酐比值(UPCR)≥1.5 gg。 |
附条件批准优先审评审批 |
|
37 |
盐酸吉卡昔替尼片 |
苏州泽璟生物制药股份有限公司 |
化学药品 |
抗肿瘤药物 |
本品适用于中危或高危原发性骨髓纤维化(PMF)、真性红细胞增多症继发性骨髓纤维化(PPV-MF)和原发性血小板增多症继发性骨髓纤维化(PET-MF)的成人患者,治疗疾病相关脾肿大或症状 。 |
|
|
38 |
盐酸来罗西利片 |
Genor Biopharma(USA), Inc. |
化学药品 |
抗肿瘤药物 |
本品联合氟维司群,适用于既往接受内分泌治疗后出现疾病进展的激素受体(HR)阳性、人表皮生长因子受体 2 (HER2)阴性晚期或转移性乳腺癌成人患者。 |
|
|
39 |
盐酸匹米替尼胶囊 |
默克雪兰诺(北 京)医药有限公 司 |
化学药品 |
抗肿瘤药物 |
本品适用于手术切除可能会导致功能受限或出现较严重并发症的症状性腱鞘巨细胞瘤(TGCT)成年患者。 |
突破性治疗优先审评审批 |
|
40 |
盐酸司美那非片 |
苏州旺山旺水生 物医药股份有限 公司 |
化学药品 |
生殖系统疾病药物 |
治疗勃起功能障碍。 |
|
|
41 |
盐酸妥诺达非片 |
扬子江药业集团 有限公司 |
化学药品 |
生殖系统疾病药物 |
治疗勃起功能障碍。 |
|
|
42 |
伊那利塞片 |
Roche Pharma(Schweiz)AG |
化学药品 |
抗肿瘤药物 |
本品联合哌柏西利和氟维司群,适用于内分泌治疗耐药 (包括在辅助内分泌治疗期间或之后出现复发)、PIK3CA突变、激素受体(HR)阳性、人表皮生长因子受体2 (HER2)阴性的局部晚期或转移性乳腺癌成人患者。 |
突破性治疗优先审评审批 |
|
43 |
泽美妥司他片 |
江苏恒瑞医药股份有限公司 |
化学药品 |
抗肿瘤药物 |
本品用于既往接受过至少1线系统性治疗的复发或难治外周T细胞淋巴瘤成人患者。 |
突破性治疗附条件批准优先审评审批 |
|
44 |
注射用磷罗 拉匹坦帕洛诺司琼 |
福建盛迪医药有限公司 |
化学药品 |
抗肿瘤药物 |
本品用于预防成人高度致吐性化疗(HEC)引起的急性和迟发性恶心和呕吐。 |
|
|
45 |
注射用盐酸伊吡诺司他 |
广州必贝特医药股份有限公司 |
化学药品 |
抗肿瘤药物 |
本品单药适用于既往接受过至少两线系统性治疗的复发或难治性弥漫性大B 细胞淋巴瘤成人患者。 |
突破性治疗附条件批准优先审评审批 |
|
46 |
宗艾替尼片 |
Boehringer Ingelheim International GmbH |
化学药品 |
抗肿瘤药物 |
本品单药适用于治疗存在HER2(ERBB2)激活突变且既往接受过至少一种系统治疗的不可切除的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。 |
突破性治疗附条件批准优先审评审批 |
|
47 |
佐来曲替尼片 |
北京诺诚健华医药科技有限公司 |
化学药品 |
抗肿瘤药物 |
本品适用于符合下列条件的成人和12 岁以上青少年实体瘤患者 - 经充分验证的检测方法诊断为携带神经营养酪氨酸受体激酶(NTRK)融 合基因且不包括已知获得性耐药突变, - 患有局部晚期、转移性疾病或手术切除可能导致严重并发症的患者,以及 -无满意替代治疗或既往治疗失败的患者。 本品为基于替代终点获得附条件批准上市,暂未获得临床终点数据,有效性和安全性尚待上市后进一步确证。 |
附条件批准优先审评审批 |
|
48 |
口服六价重 配轮状病毒 减毒活疫苗 |
武汉生物制品研 究所有限责任公 司 |
预防用生物制品 |
预防性疫苗 |
本品用于预防轮状病毒血清型G1、G2、G3、G4、G8、G9引起的婴幼儿急性胃肠炎。 |
优先审评审批 |
|
(Vero细胞) |
||||||
|
49 |
艾米迈托赛注射液 |
铂生卓越生物科 技(北京)有限 公司 |
治疗用生物制品 |
血液系统疾病药物 |
用于治疗14岁以上消化道受累为主的激素治疗失败的急性移植物抗宿主病(aGVHD)。 |
附条件批准优先审评审批 |
|
50 |
波哌达可基注射液 |
上海信致医药科技有限公司 |
治疗用生物制品 |
血液系统疾病药物 |
用于治疗中重度血友病B(先天性凝血因子Ⅸ缺乏症)成年患者。 |
突破性治疗优先审评审批 |
|
51 |
菲诺利单抗注射液 |
神州细胞工程有限公司 |
治疗用生物制品 |
抗肿瘤药物 |
本品与含铂化疗联合用于复发性和或转移性头颈部鳞状细胞癌的一线治疗。 |
|
|
本品联合贝伐珠单抗用于既往未接受过系统治疗的不可切除或转移性肝细胞癌的患者。 |
||||||
|
52 |
雷尼基奥仑赛注射液 |
上海恒润达生生 物科技股份有限 公司 |
治疗用生物制品 |
抗肿瘤药物 |
本品用于治疗经过二线或以上系统性治疗后成人复发或难治性大B细胞淋巴瘤,包括弥漫性大B细胞淋巴瘤非特指型、滤泡性淋巴瘤转化的弥漫性大B细胞淋巴瘤、伴MYC和BCL2重排的高级别B细胞淋巴瘤、高级别B细胞淋巴瘤非特指型。 |
|
|
53 |
马塔西单抗注射液 |
Pfizer Inc. |
治疗用生物制品 |
血液系统疾病药物 |
本品适用于患有以下疾病且体重 ≥ 35 kg的 12岁及以上儿童和成人患者的常规预防治疗,以防止出血或降低出血发作的频率: 不存在凝血因子VIII 抑制物的重型A型血友病(先天性凝血因子VIII 缺乏,FVIII<1%)或 不存在凝血因子IX 抑制物的重型B型血友病(先天性凝血因子IX缺乏,FIX<1%)。 |
|
|
54 |
匹康奇拜单抗注射液 |
信达生物医药科技(杭州)有限 |
治疗用生物制品 |
皮肤及五官科药物 |
本品适用于适合系统性治疗的中重度斑块状银屑病成人患者。 |
|
公司 |
||||||
|
55 |
普基奥仑赛注射液 |
重庆精准生物技术有限公司 |
治疗用生物制品 |
抗肿瘤药物 |
本品用于治疗3~21岁CD19阳性的难治或复发(首次缓解12 个月后复发需经挽救化疗)的急性B 淋巴细胞白血病患者 。 |
突破性治疗附条件批准优先审评审批 |
|
56 |
斯泰度塔单抗注射液 |
珠海泰诺麦博制药股份有限公司 |
治疗用生物制品 |
抗感染药物 |
本品为被动免疫制剂,用于成人破伤风紧急预防。 |
突破性治疗优先审评审批 |
|
57 |
依若奇单抗注射液 |
中山康方生物医药有限公司 |
治疗用生物制品 |
皮肤及五官科药物 |
本品适用于对环孢素、甲氨蝶呤(MTX)等其他系统性治疗或PUVA(补骨脂素和紫外线A)不应答、有禁忌或无法耐受的中度至重度斑块状银屑病的成年患者的治疗。 |
|
|
58 |
依苏帕格鲁 肽α注射 液 |
上海银诺医药技术有限公司 |
治疗用生物制品 |
内分泌系统疾病药物 |
本品适用于成人2 型糖尿病患者的血糖控制: 单药治疗:仅靠饮食控制和运动血糖控制不佳的患者。 联合治疗:在饮食控制和运动基础上,接受二甲双胍治疗血糖仍控制不佳的患者。 |
|
|
59 |
怡培生长激素注射液 |
厦门特宝生物工程股份有限公司 |
治疗用生物制品 |
内分泌系统疾病药物 |
本品适用于治疗3岁及以上儿童的生长激素缺乏症所致的生长缓慢。 |
|
|
60 |
重组人白蛋白注射液 (水稻) |
武汉禾元生物科技股份有限公司 |
治疗用生物制品 |
外科及其他药物 |
肝硬化低白蛋血症 (≤30gL)的治疗。 |
优先审评审批 |
|
61 |
注射用阿格司亭α |
江苏泰康生物医药有限公司 |
治疗用生物制品 |
抗肿瘤药物 |
适用于成年非髓性恶肿瘤患者在接受容易引起发热中粒细胞减少症的骨髓抑制性抗癌药物治疗时,使用本品降低以发热中粒细胞减少症为表现的感染发生率。 |
|
|
62 |
注射用博度曲妥珠单抗 |
四川科伦博泰生 物医药股份有限 公司 |
治疗用生物制品 |
抗肿瘤药物 |
本品适用于既往接受过一种或一种以上抗HER2药物治疗的不可切除或转移性HER2阳性成人乳腺癌患者。 |
|
|
63 |
注射用德达博妥单抗 |
DaiichiSankyoEurope GmbH |
治疗用生物制品 |
抗肿瘤药物 |
本品用于治疗既往接受过内分泌治疗且在晚期疾病阶段接受过至少一线化疗的不可切除或转移性的激素受体 |
|
(HR)阳性、人类表皮生长因子受体2(HER2)阴性(IHC 0、IHC1+或IHC 2+ISH-)乳腺癌成人患者。 |
||||||
|
64 |
注射用伏欣奇拜单抗 |
长春金赛药业有限责任公司 |
治疗用生物制品 |
风湿性疾病及免疫药物 |
本品适用于对非甾体类抗炎药和或秋水仙碱禁忌、不耐受或缺乏疗效的,以及不适合反复使用类固醇激素的成人痛风性关节炎急性发作。 |
|
|
65 |
注射用瑞卡西单抗 |
广东恒瑞医药有限公司 |
治疗用生物制品 |
循环系统疾病药物 |
在控制饮食的基础上,与他汀类药物、或者与他汀类药物及其他降脂疗法联合用药,用于接受中等或以上剂量他汀类药物治疗,仍无法达到低密度脂蛋白胆固醇(LDL-C)目标的原发性高胆固醇血症(包括杂合子型家族性和非家族性高胆固醇血症)和混合型血脂异常的成人患者;或单药用于非家族性高胆固醇血症和混合型血脂异常的成人患者,以降低低密度脂蛋白胆固醇(LDL-C)、总胆固醇 (TC)、载脂蛋白 B(ApoB)水平。 |
|
|
66 |
注射用瑞康曲妥珠单抗 |
苏州盛迪亚生物医药有限公司 |
治疗用生物制品 |
抗肿瘤药物 |
本品单药适用于治疗存在HER2(ERBB2)激活突变且既往接受过至少一种系统治疗的不可切除的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。 |
突破性治疗附条件批准优先审评审批 |
|
67 |
注射用苏维西塔单抗 |
江苏先声生物制药有限公司 |
治疗用生物制品 |
抗肿瘤药物 |
苏维西塔单抗联合紫杉醇、多柔比星脂质体或拓扑替康用于铂耐药后接受过不超过1 种系统治疗的成人复发性卵巢癌、输卵管癌或原发性腹膜癌的治疗。 |
|
|
68 |
注射用维贝柯妥塔单抗 |
乐普生物科技股份有限公司 |
治疗用生物制品 |
抗肿瘤药物 |
本品适用于治疗既往经至少二线系统化和 PD-1PD-L1 抑制剂治疗失败的 抑制剂治疗失败的 复发转移性鼻咽癌的成人患者。 |
突破性治疗附条件批准优先审评审批 |
|
69 |
注射用维拉苷酶β |
北海康成(上 海)生物科技有 限公司 |
治疗用生物制品 |
内分泌系统疾病药物 |
适用于12岁及以上青少年和成人Ⅰ型和Ⅲ型戈谢病患者的长期酶替代治疗(ERT)。 |
优先审评审批 |
|
70 |
注射用泽尼 |
百济神州(苏 |
治疗用生 |
抗肿瘤药物 |
本品适用于既往接受过全身治疗的HER2高表达 |
突破性治疗 |
|
达妥单抗 |
州)生物科技有限公司 |
物制品 |
(IHC3+)的不可切除局部晚期或转移性胆道癌患者。 |
附条件批准优先审评审批 |
||
|
71 |
参蒲颗粒 |
江苏康缘药业股份有限公司 |
中药 |
妇科 |
益气活血,清利湿热,通络止痛。用于盆腔炎性疾病后遗症引起的慢性盆腔痛中医辨证属湿热瘀阻证,症见下腹隐痛、腰骶胀痛、白带量多色黄、经行腹痛加重、胸闷纳 呆、口干等,舌体胖大,色红,苔黄腻,脉弦数或滑数。 |
|
|
72 |
复方比那甫西颗粒 |
新疆银朵兰药业股份有限公司 |
中药 |
呼吸 |
清除体内异常液质,用于热性感冒,症见发热、鼻塞、流涕、咽痛、头痛、口干等。 |
|
|
73 |
芪防鼻通片 |
北京以岭药业有限公司 |
中药 |
皮肤及五官科药物 |
益气通窍。用于改善肺脾两虚型持续性变应鼻炎 未合并季节性过 敏原者的喷嚏、流涕鼻痒塞,舌淡苔白脉浮或细弱。 |
|
|
74 |
小儿黄金止咳颗粒 |
北京东方运嘉药业有限公司 |
中药 |
呼吸 |
清肺化痰,肃肺止咳。用于儿童轻度急性支气管炎痰热阻肺证引起的咳嗽,舌红苔薄黄或黄腻。 |
优先审评审批 |
|
75 |
小儿牛黄退热贴膏 |
健民药业集团股份有限公司 |
中药 |
呼吸 |
退热解表,清热解毒。用于小儿急性上呼吸道感染风热证所致的发热(38.5℃及以下) |
|
|
76 |
养血祛风止痛颗粒 |
广东方盛健盟药业有限公司 |
中药 |
精神神经 |
补气养血,散风止痛。用于频发性紧张型头痛中医辨证属气血两虚证,症见头痛反复发作、头脑昏沉,以及食少纳呆、自汗、气短、神疲乏力、面色苍白,舌淡苔白、脉沉细而弱等。 |
附件2 2025 年通过优先审评审批程序批准的罕见病用药
2025 年通过优先审评审批程序批准的罕见病用药
|
序号 |
药品名称 |
上市许可持有人 |
药品类型 |
注册分类 |
适应症 |
|
1 |
阿夫凯泰片 |
Cytokinetics, Incorporated |
化学药品 |
1 |
本品用于治疗纽约心脏协会(NYHA)心功能分级II-III级的梗阻性肥厚型心肌病(HCM)成人患者,以改善运动能力和症状。 |
|
2 |
芦沃美替尼片 |
上海复星医药产业发展有限公司 |
化学药品 |
1 |
朗格汉斯细胞组织细胞增生症和组织细胞肿瘤:本品适用于朗格汉斯细胞组织细胞增生症(LCH)和组织细胞肿瘤成人患者。伴有症状、无法手术的丛状神经纤维瘤的I 型神经纤维瘤病:本品适用于2岁及2岁以上伴有症状、无法手术的丛状神经纤维瘤 (PN)的 I型神经纤维瘤病(NF1)儿童及青少年患者。 |
|
3 |
那米司特片 |
Boehringer Ingelheim International GmbH |
化学药品 |
1 |
用于治疗特发性肺纤维化(IPF)成人患者。用于治疗进展性肺纤维化(PPF)成人患者。 |
|
4 |
盐酸匹米替尼胶囊 |
默克雪兰诺(北 京)医药有限公 司 |
化学药品 |
1 |
本品适用于手术切除可能会导致功能受限或出现较严重并发症的症状性腱鞘巨细胞瘤(TGCT)成年患者。 |
|
5 |
乌帕替尼缓释片 |
AbbVie Deutschland GmbH &Co.KG |
化学药品 |
2.4 |
本品适用于巨细胞动脉炎成人患者。使用限制:不建议本品与其他JAK 抑制剂、生物类DMARD 或强效免疫抑制剂(如硫唑嘌呤和环孢素)联合使用。 |
|
6 |
巴氯芬口服溶液 |
成都倍特得诺药业有限公司 |
化学药品 |
3 |
适用于多发性硬化症所引起的严重但可逆的肌肉痉挛。对感染 性、退行性、外伤性、肿瘤或原因不明的脊髓疾病引起的痉挛可能有一定的疗效。 |
|
序号 |
药品名称 |
上市许可持有人 |
药品类型 |
注册分类 |
适应症 |
|
7 |
注射用双羟 萘酸帕瑞肽微球 |
Recordati RareDiseases |
化学药品 |
5.1 |
本品用于治疗无法手术或手术未治愈,且通过另一种生长抑素类似物治疗控制不佳的成人肢端肥大症患者。 |
|
8 |
波哌达可基注射液 |
上海信致医药科技有限公司 |
治疗用生物制品 |
1 |
用于治疗中重度血友病B(先天凝血因子IX 缺乏症)成年患者 |
|
9 |
注射用维拉苷酶β |
北海康成(上 海)生物科技有 限公司 |
治疗用生物制品 |
1 |
适用于12岁及以上青少年和成人Ⅰ型和Ⅲ型戈谢病患者的长期酶替代治疗(ERT)。 |
|
10 |
伊奈利珠单抗注射液 |
Horizon Therapeutics Ireland DAC |
治疗用生物制品 |
2.2 |
本品适用于免疫球蛋白G4 相关性疾病(IgG4-RD)成人患者。 |
|
11 |
注射用泰它西普 |
荣昌生物制药 (烟台)股份有 限公司 |
治疗用生物制品 |
2.2 |
本品与常规治疗药物联合,用于治疗抗乙酰胆碱受体(AChR)抗体阳性的成人全身型重症肌无力(gMG)患者。 |
|
12 |
注射用卡拉西珠单抗 |
Ablynx NV |
治疗用生物制品 |
3.1 |
本品适用于与血浆置换和免疫抑制疗法联合治疗获得性血栓性血小板减少性紫癜(aTTP)(也称为免疫介导的血栓性血小板减少性紫癜(iTTP))的成人和 12岁及以上体重至少40 kg的青少年患者。 |
2025 年通过优先审评审批程序批准的儿童用药
|
序号 |
药品名称 |
上市许可持有人 |
药品类型 |
注册 分类 |
适应症/功能主治 |
|
1 |
芦沃美替尼片 |
上海复星医药产业发展有限公司 |
化学药品 |
1 |
2岁及2岁以上伴有症状、无法手术的丛状神经纤维瘤(PN)的 I型神经纤维瘤病(NF1)儿童及青少年患者 |
|
2 |
佐来曲替尼片 |
北京诺诚健华医药科技有限公司 |
化学药品 |
1 |
本品适用于符合下列条件的成人和12岁以上青少年实体瘤患者 - 经充分验证的检测方法诊断为携带神经营养酪氨酸受体激酶(NTRK)融合基因且不包括已知获得性耐药突变, - 患有局部晚期、转移性疾病或手术切除可能导致严重并发症的患者,以及 - 无满意替代治疗或既往治疗失败的患者。 本品为基于替代终点获得附条件批准上市,暂未获得临床终点数据,有效性和安全性尚待上市后进一步确证。 |
|
3 |
马来酸噻吗洛尔凝胶 |
北京梅尔森医药技术开发有限公司 |
化学药品 |
2.2,2.4 |
用于增殖期浅表性婴儿血管瘤的治疗。 |
|
4 |
巯嘌呤片 (II) |
华润双鹤药业股份有限公司 |
化学药品 |
2.2 |
适用于儿童急性淋巴细胞白血病(ALL)及急性非淋巴细胞白血病,慢性粒细胞白血病的急变期。 |
|
5 |
巴氯芬口服溶液 |
成都倍特得诺药业有限公司 |
化学药品 |
3 |
适用于多发性硬化症所引起的严重但可逆的肌肉痉挛。 对感染性、退行性、外伤性、肿瘤或原因不明的脊髓疾病引起的痉挛可能有一定的疗效。 |
|
序号 |
药品名称 |
上市许可持有人 |
药品类型 |
注册 分类 |
适应症/功能主治 |
|
6 |
复方磺胺甲噁唑注射液 |
华夏生生药业(北京)有限公司 |
化学药品 |
3 |
1、适用于治疗成人和2 个月以上小儿的肺孢子菌肺炎。 2、适用于治疗成人和2 个月以上小儿由福氏或宋内志贺菌敏感菌株引起的肠炎。 3、当无法口服复方磺胺甲噁唑,且机体对尿路中有效的单方抗菌 药物不敏感时,本品适用于治疗成人和2 个月以上小儿由大肠埃希菌、克雷伯菌属、肠杆菌属、摩根菌属、奇异变形杆菌和普通变形杆菌敏感菌株所致的严重或复杂尿路感染。 |
|
7 |
吗替麦考酚酯干混悬剂 |
杭州中美华东制药有限公司 |
化学药品 |
3 |
本品与皮质类固醇以及环孢素或他克莫司同时应用,适用于治疗: • 接受同种异体肾脏移植的患者中预防器官的排斥反应。 • 接受同种异体肝脏移植的患者中预防器官的排斥反应。 本品适用于III-V型成人狼疮性肾炎患者的诱导期治疗和维持期治疗。 |
|
8 |
肾上腺素注射液 |
武汉久安药物研究院 有限公司 |
化学药品 |
3 |
主要适用于因支气管痉挛所致严重呼吸困难,可迅速缓解药物等引起的过敏性休克,亦可用于延长浸润麻醉用药的作用时间。各种原因引起的心脏骤停进行心肺复苏的主要抢救用药。 |
|
9 |
肾上腺素注射液 |
成都诺和晟鸿生物制药有限公司 |
化学药品 |
3 |
主要适用于因支气管痉挛所致严重呼吸困难,可迅速缓解药物等引起的过敏性休克,亦可用于延长浸润麻醉用药的作用时间。各种原因引起的心脏骤停进行心肺复苏的主要抢救用药。 |
|
10 |
托吡酯口服溶液 |
海南斯达制药有限公 司 |
化学药品 |
3 |
本品用于初诊为癫痫的患者的单药治疗或曾经合并用药现转为单药治疗的癫痫患者。 本品用于成人及2~16岁儿童部分性癫痫发作的加用治疗。 |
|
11 |
维生素K₁注射液 |
海南倍特药业有限公 司 |
化学药品 |
3 |
用于预防和治疗婴儿维生素K 缺乏性出血。 |
|
序号 |
药品名称 |
上市许可持有人 |
药品类型 |
注册 分类 |
适应症/功能主治 |
|
12 |
维生素K₁注射液 |
合肥亿帆生物制药有限公司 |
化学药品 |
3 |
用于预防和治疗婴儿维生素K 缺乏性出血。 |
|
13 |
盐酸胍法辛缓释片 |
四川百利药业有限责任公司 |
化学药品 |
3 |
本品用于治疗6岁及6岁以上注意缺陷多动障碍(ADHD)。 |
|
14 |
盐酸右哌甲酯缓释胶囊 |
河南中帅药业有限公 司 |
化学药品 |
3 |
本品用于治疗6岁及6岁以上注意缺陷多动障碍(ADHD)。 |
|
15 |
复方氯丝右哌甲酯胶囊 |
Commave TherapeuticsSA |
化学药品 |
5.1 |
本品用于6岁及6岁以上注意缺陷多动障碍(ADHD)患者的治疗。 |
|
16 |
来特莫韦片(Ⅱ) |
MerckSharp & Dohme LLC,a subsidiaryofMerck& Co.,Inc. |
化学药品 |
5.1 |
本品用于接受异基因造血干细胞移植(HSCT)的巨细胞病毒 (CMV)血清学阳性的成人和6 个月及以上且体重≥6kg的儿童受者[R+]预防巨细胞病毒感染和巨细胞病毒病。 |
|
17 |
褪黑素颗粒 |
Nobelpharma Co., Ltd. |
化学药品 |
5.1 |
用于改善6-15岁神经发育障碍儿童的入睡困难。 |
|
18 |
口服六价重配 轮状病毒减毒 活疫苗(Vero 细胞) |
武汉生物制品研究所 有限责任公司 |
预防用生物制品 |
1.4 |
本品用于预防轮状病毒血清型G1、G2、G3、G4、G8、G9引起的婴幼儿急性胃肠炎。 |
|
19 |
艾米迈托赛注射液 |
铂生卓越生物科技(北京)有限公司 |
治疗用生物制品 |
1 |
用于治疗14岁以上消化道受累为主的激素治疗失败的急性移植物抗宿主病(aGVHD)。 本适应症为附条件批准上市,更多的有效性和安全性数据待上市后研究提供。 |
|
序号 |
药品名称 |
上市许可持有人 |
药品类型 |
注册 分类 |
适应症/功能主治 |
|
20 |
普基奥仑赛注射液 |
重庆精准生物技术有限公司 |
治疗用生物制品 |
1 |
本品用于治疗3~21岁CD19阳性的难治或复发(首次缓解12 个月后复发需经挽救化疗)的急性B 淋巴细胞白血病患者。本适应症为附条件批准上市,更多的有效性和安全性数据待上市后研究提供。 |
|
21 |
注射用维拉苷酶β |
北海康成(上海)生物科技有限公司 |
治疗用生物制品 |
1 |
适用于12岁及以上青少年和成人Ⅰ型和Ⅲ型戈谢病患者的长期酶替代治疗(ERT)。 |
|
22 |
替利珠单抗注射液 |
Provention Bio, Inc. |
治疗用生物制品 |
3.1 |
本品适用于8岁(含)以上儿童和成人1型糖尿病2 期患者,以延缓向1型糖尿病3期进展。 |
|
23 |
注射用卡拉西珠单抗 |
Ablynx NV |
治疗用生物制品 |
3.1 |
本品适用于与血浆置换和免疫抑制疗法联合治疗获得性血栓性血小板减少性紫癜(aTTP)(也称为免疫介导的血栓性血小板减少性紫癜(iTTP))的成人和 12岁及以上体重至少40 kg的青少年患者。 |
|
24 |
小儿黄金止咳颗粒 |
北京东方运嘉药业有限公司 |
中药 |
1.1 |
清肺化痰,肃肺止咳。用于儿童轻度急性支气管炎痰热阻肺证引起的咳嗽,舌红苔薄黄或黄腻。 |
|
25 |
菖麻熄风颗粒 |
黑龙江省济仁药业有限公司 |
中药 |
2.2 |
平肝熄风,安神化痰。用于轻中度小儿多发性抽动症属中医肝风内动挟痰证者。症见头、颈、五官或肢体不自主抽动,喉中发出异常声音,烦躁易怒,多梦易惊,舌红苔白腻,脉弦滑等。 |
附件4 2025 年国家药监局批准的境外已上市境内未上市的药品
2025 年国家药监局批准的境外已上市境内未上市的药品
|
序号 |
药品名称 |
上市许可持有人 |
药品类型 |
注册分类 |
适应症 |
首次批准上 市/增加适应 症 |
|
1 |
阿达帕林 过氧苯甲酰凝胶 |
GaldermaSA |
化学药品 |
5.1 |
本品适用于伴粉刺、丘疹和脓疱的寻常痤疮的皮肤治疗。本品适用于成人、青少年和9岁及以上儿童。 |
首次批准上市 |
|
2 |
奥洛他定 莫米松鼻喷雾剂 |
GLENMARKSPECIALTY SA |
化学药品 |
5.1 |
成人和6岁及以上儿童的中度至重度季节性过敏性鼻炎的对症治疗;成人和12岁及以上儿童的中度至重度常年性过敏性鼻炎的对症治疗 |
首次批准上市 |
|
3 |
雌二醇透皮喷雾剂 |
Gedeon Richter Plc. |
化学药品 |
5.1 |
适用于绝经后女性(末次月经后闭经至少6 个月;或手术绝经的女性,无论有或无子宫)雌激素缺乏症状的激素替代治疗。 本品在65岁以上女性中的治疗经验有限。 |
首次批准上市 |
|
4 |
厄达替尼片 |
Janssen Biotech, Inc. |
化学药品 |
5.1 |
本品用于携带易感型FGFR3 基因变异,且既往接受至少一线含抗PD-1 或抗PD-L1 期间或之后出现疾病进展的手术不可切除的局部晚期或转移性尿路上皮癌(UC)成人患者。 |
首次批准上市 |
|
5 |
恩考芬尼胶囊 |
PIERRE FABREMEDICAMENT |
化学药品 |
5.1 |
恩考芬尼联合西妥昔单抗用于治疗既往接受过全身治疗的BRAFV600E突变型转移性结直肠癌(CRC)成人患者。 |
首次批准上市 |
|
6 |
二十碳五 烯酸乙酯软胶囊 (Ⅱ) |
Mochida Pharmaceutical CO.,LTD. |
化学药品 |
5.1 |
在控制饮食的基础上, 本品用于降低重度高甘油三酯血症(≥500mg/dL) 成年患者的甘油三酯(TG) 水平。尚未评估本品对重度高甘油三酯血症患者发生胰腺炎风险的影响。 |
首次批准上市 |
|
7 |
非那雄胺喷雾剂 |
Polichem S.A. |
化学药品 |
5.1 |
本品适用于18至41岁男性轻度至中度男性型秃发(雄激素性秃发)的局部外用治疗,以促进头发生长并防止继续脱发。 |
首次批准上市 |
|
序号 |
药品名称 |
上市许可持有人 |
药品类型 |
注册分类 |
适应症 |
首次批准上 市/增加适应 症 |
|
8 |
复方氯丝 右哌甲酯胶囊 |
Commave TherapeuticsSA |
化学药品 |
5.1 |
本品用于6岁及6岁以上注意缺陷多动障碍(ADHD)患者的治疗。 |
首次批准上市 |
|
9 |
睾酮凝胶 |
Besins Healthcare S.A. |
化学药品 |
5.1 |
本品适用于成年男性的睾酮替代疗法,用于治疗经临床指征和生物学检验确诊为男性性腺功能减退的成年男性患者 |
首次批准上市 |
|
10 |
枸橼酸艾瑞芬净片 |
SCYNEXIS Inc. |
化学药品 |
5.1 |
用于成年和初潮后青少女性的外阴阴道念珠菌病(VVC)的治疗。 如果在治疗前获得真菌培养标本,可在得知培养结果之前进行抗真菌治疗。一旦获得培养结果,应相应地调整抗真菌治疗。 |
首次批准上市 |
|
11 |
枸橼酸西 地那非口 服混悬液 |
Farmalider,S.A. |
化学药品 |
5.1 |
用于治疗勃起功能障碍 |
首次批准上市 |
|
12 |
环丙沙星 氟轻松滴耳液 |
LABORATORIOS SALVAT,S.A. |
化学药品 |
5.1 |
用于治疗7 岁及7 岁以上儿童和成人由环丙沙星敏感菌导致的急性外耳炎(AOE) |
首次批准上市 |
|
13 |
环索奈德 吸入气雾剂 |
Covis Pharma GmbH |
化学药品 |
5.1 |
作为一种预防性治疗措施用于成人、青少年和6岁及以上儿童支气管哮喘患者的维持治疗。 |
首次批准上市 |
|
14 |
来特莫韦片(Ⅱ) |
Merck Sharp& Dohme LLC,a subsidiaryofMerck & Co.,Inc. |
化学药品 |
5.1 |
本品用于接受异基因造血干细胞移植(HSCT)的巨细胞病毒 CMV)血清学阳性的成人和 6 个月及以上且体重≥6kg的儿童受者 [R+]预防巨细胞病毒感染和巨细胞病毒病。 |
首次批准上市 |
|
序号 |
药品名称 |
上市许可持有人 |
药品类型 |
注册分类 |
适应症 |
首次批准上 市/增加适应 症 |
|
15 |
莱博雷生片 |
Eisai Co.,Ltd. |
化学药品 |
5.1 |
本品适用于治疗以入睡困难和/或睡眠维持困难为特征的成人失眠患者。 |
首次批准上市 |
|
16 |
硫糖铝口 服混悬凝胶 |
Laboratorio Italiano Biochimico Farmaceutico LisapharmaS.p.A. |
化学药品 |
5.1 |
本品适用于治疗胃溃疡、十二指肠溃疡、有症状的慢性胃炎。 |
首次批准上市 |
|
17 |
佩玛贝特片 |
Kowa Company, Ltd. |
化学药品 |
5.1 |
在控制饮食的基础上,本品用于非家族型高甘油三酯血症成年患者以降低甘油三酯(TG)水平。 |
首次批准上市 |
|
18 |
氢溴酸他 泽司他片 |
Epizyme, Inc. |
化学药品 |
5.1 |
本品单药用于既往接受过至少两种系统性治疗后的EZH2突变阳性复发或难治性滤泡性淋巴瘤 (FL) 成人患者。 |
首次批准上市 |
|
19 |
瑞维那新 吸入溶液 |
Mylan Ireland Limited |
化学药品 |
5.1 |
本品适用于慢性阻塞性肺疾病(COPD)患者的维持治疗。 |
首次批准上市 |
|
20 |
肾上腺素鼻喷雾剂 |
ARS PharmaceuticalsOperations, Inc. |
化学药品 |
5.1 |
用于成人及体重≥30kg儿童的I型过敏反应包括严重过敏反应的紧急治疗。 |
首次批准上市 |
|
21 |
他氟噻吗滴眼液 |
Santen Oy |
化学药品 |
5.1 |
降低开角型青光眼或高眼压症患者的眼压,用于对局部单独使用β-受体阻滞剂或前列腺素衍生物疗效不佳而需要联合治疗,及对使用无防腐剂滴眼液可能获益的患者。 |
首次批准上市 |
|
22 |
咕诺美林 曲司氯铵胶囊(I)/ |
Bristol-MyersSquibb Company |
化学药品 |
5.1 |
本品用于治疗成人精神分裂症。 |
首次批准上市 |
|
序号 |
药品名称 |
上市许可持有人 |
药品类型 |
注册分类 |
适应症 |
首次批准上 市/增加适应 症 |
|
(II)/ (III) |
||||||
|
23 |
褪黑素颗粒 |
NobelpharmaCo., Ltd. |
化学药品 |
5.1 |
用于改善 6-15 岁神经发育障碍儿童的入睡困难。 |
首次批准上市 |
|
24 |
维生素K₁滴剂 |
NeoceuticalsLimited |
化学药品 |
5.1 |
用于预防婴儿维生素 K 缺乏性出血 |
首次批准上市 |
|
25 |
西诺氨酯片 |
SK LifeScience, Inc. |
化学药品 |
5.1 |
本品适用于成人癫痫患者部分性发作的治疗。 |
首次批准上市 |
|
26 |
盐酸氨溴 索口服溶液 |
A. Nattermann &Cie. GmbH |
化学药品 |
5.1 |
本品适用于痰液粘稠不易咳出者。本品用于急、慢性支气管炎引起的痰液粘稠、咳痰困难。 |
首次批准上市 |
|
27 |
盐酸达利雷生片 |
Idorsia Pharmaceuticals Deutschland GmbH |
化学药品 |
5.1 |
本品适用于治疗以入睡困难和/或睡眠维持困难为特征的成人失眠患者。 |
首次批准上市 |
|
28 |
盐酸菲优拉生片 |
Daewoong Pharmaceutical Co., Ltd. |
化学药品 |
5.1 |
反流性食管炎。 |
首次批准上市 |
|
29 |
盐酸沙瑞环素片 |
Almirall, LLC |
化学药品 |
5.1 |
本品用于 9 岁及以上患者的非结节性中度至重度寻常痤疮炎症性病变的治疗。本品超过 12 周的有效性和超过12 个月的安全性尚未确立。 本品未在感染治疗方面进行过评估,为了减少耐药菌的产生并保持其他抗菌药物的有效性,本品应仅按照适应症使用 |
首次批准上市 |
|
序号 |
药品名称 |
上市许可持有人 |
药品类型 |
注册分类 |
适应症 |
首次批准上 市/增加适应 症 |
|
30 |
盐酸索安非托片 |
AXSOME MALTA LTD. |
化学药品 |
5.1 |
用于改善阻塞性睡眠呼吸暂停(OSA)伴有日间过度嗜睡(EDS)的成人患者的觉醒程度。 使用限制:使用前应确保OSA主要治疗方法维持足够的治疗时间,治疗期间应继续采用OSA主要治疗方法治疗气道阻塞。 |
首次批准上市 |
|
31 |
眼内注射 用曲安奈德 |
WAKAMOTO PHARMACEUTICA L CO., LTD. |
化学药品 |
5.1 |
玻璃体手术时的玻璃体可视化。 |
首次批准上市 |
|
32 |
依普隆特 生钠注射液 |
AstraZeneca AB |
化学药品 |
5.1 |
本品适用于治疗成人遗传性转甲状腺素蛋白淀粉样变性多发性神经病(ATTRv-PN)患者 |
首次批准上市 |
|
33 |
乙酰半胱 氨酸注射液 |
ZambonSwitzerland Ltd |
化学药品 |
5.1 |
治疗浓稠粘液分泌物过多的呼吸道疾病如:急性支气管炎、慢性支气管炎及其病情恶化者、肺气肿、粘稠物阻塞症以及支气管扩张症。 |
首次批准上市 |
|
34 |
泽卢克布 仑钠注射液 |
UCB PharmaS.A. |
化学药品 |
5.1 |
本品与常规治疗药物联合用于治疗抗乙酰胆碱受体(AChR)抗体阳性的成人全身型重症肌无力(gMG)患者。 |
首次批准上市 |
|
35 |
注射用镓[68Ga]戈泽肽药盒 |
NovartisPharma SchweizAG |
化学药品 |
5.1 |
本品为药物制剂的配套药盒,用氯化镓[68Ga]洗脱液进行放射性标记后制成放射性药物制剂镓[68Ga]戈泽肽注射液,适用于通过正电子发射断层成像(PET)识别前列腺癌男性患者的前列腺特异性膜抗原(PSMA)阳性病灶,根据治疗性产品说明书中相关要求,选择适用于PSMA 靶向治疗的前列腺癌患者。 |
首次批准上市 |
|
序号 |
药品名称 |
上市许可持有人 |
药品类型 |
注册分类 |
适应症 |
首次批准上 市/增加适应 症 |
|
36 |
注射用双 羟萘酸帕 瑞肽微球 |
Recordati RareDiseases |
化学药品 |
5.1 |
本品用于治疗无法手术或手术未治愈,且通过另一种生长抑素类似物治疗控制不佳的成人肢端肥大症患者。 |
首次批准上市 |
|
37 |
注射用头孢洛生他唑巴坦钠 |
Merck Sharp&Dohme B.V. |
化学药品 |
5.1 |
复杂性腹腔感染 本品与甲硝唑联合适用于在成人和儿童(出生至18岁以下)患者中治疗以下敏感革兰阴性和革兰阳性微生物引起的复杂性腹腔感染(cIAI):阴沟肠杆菌、大肠埃希菌、产酸克雷伯菌、肺炎克雷伯菌、奇异变形杆菌、铜绿假单胞菌、脆弱拟杆菌、咽峡炎链球菌、星座链球菌和唾液链球菌。 复杂性尿路感染,包括肾盂肾炎 本品适用于在成人和儿童(出生至 18岁以下)患者中治疗以下敏感革兰阴性微生物引起的复杂性尿路感染(cUTI)(包括肾盂肾炎):大肠埃希菌、肺炎克雷伯菌、奇异变形杆菌和铜绿假单胞菌。 医院获得性细菌性肺炎和呼吸机相关性细菌性肺炎 本品适用于在成人(18岁及以上)患者中治疗以下敏感革兰阴性微生物引起的医院获得性细菌性肺炎(HABP)和呼吸机相关性细菌性肺炎(VABP):阴沟肠杆菌、大肠埃希菌、流感嗜血杆菌、产酸克雷伯菌、肺炎克雷伯菌、奇异变形杆菌、铜绿假单胞菌和粘质沙雷菌。 |
首次批准上市 |
|
38 |
注射用托 伐普坦磷酸钠 |
Otsuka Pharmaceutical Co., Ltd. |
化学药品 |
5.1 |
用于袢利尿剂等其他利尿剂治疗效果不理想的心力衰竭引起的体液潴留。 |
首次批准上市 |
|
序号 |
药品名称 |
上市许可持有人 |
药品类型 |
注册分类 |
适应症 |
首次批准上 市/增加适应 症 |
|
39 |
注射用盐 酸替拉凡 星 |
Cumberland Pharmaceuticals Inc. |
化学药品 |
5.1 |
本品仅在其他治疗不适用时,用于由金黄色葡萄球菌敏感分离株引起的医院获得性和呼吸机相关细菌肺炎(HABP/VABP)。 为减少耐药菌的产生并维持本品和其他抗菌药物的有效性, 本品应仅用于治疗已确诊或高度怀疑由敏感菌引起的感染。如可获得细菌培养和药物敏感性结果,应当考虑据此选择或调整药 物。在缺乏此类数据的情况下,当地流行病学资料和药物敏感性分析可能有助于经验性选择治疗。 替拉凡星不适用于治疗革兰氏阴性菌感染。如确诊或疑诊合并革兰氏阴性菌感染,应立即开始针对性的抗革兰氏阴菌治疗。 |
首次批准上市 |
|
40 |
镥[¹了了Lu]特昔维匹肽注射液 |
NovartisPharma SchweizAG |
化学药品 |
5.1 |
本品适用于以下成人患者:既往接受雄激素受体通路抑制和紫杉类化疗后疾病进展的前列腺特异性膜抗原(PSMA)阳性转移性去势抵抗性前列腺癌(mCRPC)。本品适用于以下成人患者:既往接受雄激素受体通路抑制剂(ARPI)后疾病进展且适合延迟化疗的前列腺特异性膜抗原(PSMA)阳性转移性去势抵抗性前列腺癌(mCRPC)。 |
首次批准上 市、增加适 应症 |
|
41 |
阿可替尼胶囊 |
AstraZenecaPtyLtd |
化学药品 |
5.1 |
本品单药适用于成人慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)患者。 |
增加适应症 |
|
42 |
奥拉帕利片 |
AstraZeneca AB |
化学药品 |
5.1 |
奥拉帕利联合阿比特龙和泼尼松或泼尼松龙用于携带胚系或体细胞BRCA突变(gBRCAm或sBRCAm)的转移性去势抵抗性前列腺癌(mCRPC)成人患者的治疗。 |
增加适应症 |
|
43 |
八氟丙烷 脂质微球注射液 |
LANTHEUS MICANADA INC |
化学药品 |
5.1 |
本品用于成人患者的肝脏超声造影。 |
增加适应症 |
|
序号 |
药品名称 |
上市许可持有人 |
药品类型 |
注册分类 |
适应症 |
首次批准上 市/增加适应 症 |
|
44 |
马来酸阿 可替尼片 |
AstraZeneca Pty Ltd |
化学药品 |
5.1 |
本品单药适用于成人慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)患者 |
增加适应症 |
|
45 |
瑞普替尼胶囊 |
Bristol-MyersSquibb Company |
化学药品 |
5.1 |
NTRK融合基因阳性实体瘤 本品适用于具有以下特征的成人实体瘤患者: ‒ 经充分验证的检测方法诊断为携带神经营养酪氨酸受体激酶(NTRK)融合基因 ‒ 患有局部晚期或转移性疾病或手术切除可能导致严重并发症的患者,以及 ‒既往治疗失败或无满意替代治疗的患者。 本品为基于替代终点获得附条件批准上市,暂未获得临床终点数据,有效性和安全性尚待上市后进一步确证。 |
增加适应症 |
|
46 |
塞利尼索片 |
Karyopharm Therapeutics Inc. |
化学药品 |
5.1 |
本品与硼替佐米和地塞米松联用,适用于既往接受过至少一线治疗的多发性骨髓瘤成人患者。 2)本品与地塞米松联用,适用于既往接受过治疗且对至少一种蛋白酶体抑制剂,一种免疫调节剂以及一种抗CD38单抗难治的复发或难治性多发性骨髓瘤成人患者。 |
增加适应症 |
|
47 |
替尔泊肽注射液 |
Eli Lilly Nederland B.V. |
化学药品 |
5.1 |
在饮食控制和运动基础上,联合胰岛素(伴或不伴口服降糖药)治疗,改善成人2型糖尿病患者的血糖控制。 |
增加适应症 |
|
48 |
维奈克拉片 |
AbbVie Inc. |
化学药品 |
5.1 |
本品单药用于既往至少经过一种治疗的伴17P 缺失的成人慢性淋巴细胞白血病或小淋巴细胞淋巴瘤患者。 |
增加适应症 |
|
49 |
盐酸卡马替尼片 |
NovartisPharma SchweizAG |
化学药品 |
5.1 |
本品用于治疗携带间质上皮转化因子(MET)外显子14跳跃突变的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。 |
增加适应症 |
|
序号 |
药品名称 |
上市许可持有人 |
药品类型 |
注册分类 |
适应症 |
首次批准上 市/增加适应 症 |
|
50 |
盐酸伊普 可泮胶囊 |
NovartisPharma SchweizAG |
化学药品 |
5.1 |
用于阵发性睡眠性血红蛋白尿症(PNH)成人患者。 |
增加适应症 |
|
51 |
九价人乳 头瘤病毒 疫苗(酿 酒酵母) |
Merck Sharp&Dohme LLC |
预防用生物制品 |
3.1 |
本品适用于16~26 岁男性预防由HPV6型、11型、16型、 18型引起的下列疾病:由 HPV 6 型、11型引起的生殖器疣(尖锐湿疣);由HPV16型、18 型引起的肛门癌;由 HPV6型、11型、16型、18 型引起的以下癌前病变或不典型病变:1 级、 2级、3级肛门上皮内瘤样病变(AIN)。 |
增加接种对象 |
|
52 |
四价人乳 头瘤病毒 疫苗(酿 酒酵母) |
Merck Sharp&Dohme LLC |
预防用生物制品 |
3.1 |
本品适用于 9~26 岁男性预防因本品所含 HPV型别所致疾 病:由 HPV16、18 型引起的肛门癌;由 HPV 6、11型引起的生殖器疣(尖锐湿疣);由HPV 6、11、16、18 型引起的以下癌前病变或不典型病变:1 级、2 级、3级肛门上皮内瘤样病变(AIN)。 |
增加接种对象 |
|
53 |
重组带状 疱疹疫苗 (CHO细 胞) |
GlaxoSmithKlineBiologicalsSA |
预防用生物制品 |
3.1 |
由已知疾病或治疗(如自体造血干细胞移植)引起的免疫缺陷或免疫抑制而导致带状疱疹风险增加的18岁及以上成人。 |
增加接种对象 |
|
54 |
阿替利珠单抗注射液(皮下注射) |
Roche Pharma (Schweiz) AG |
治疗用生物制品 |
3.1 |
本品与卡铂和依托泊苷联合用于广泛期小细胞肺癌(ES-SCLC)患者的一线治疗。 肝细胞癌 本品联合贝伐珠单抗治疗既往未接受过全身系统性治疗的不可切除肝细胞癌患者。 早期非小细胞肺癌 阿替利珠单抗单药用于经国家药品监督管理局批准的检测方法评 |
首次批准上市 |
|
序号 |
药品名称 |
上市许可持有人 |
药品类型 |
注册分类 |
适应症 |
首次批准上 市/增加适应 症 |
|
估为≥1%肿瘤细胞(TC)PD-L1 染色阳性、经手术切除、以铂类为基础化疗之后的II-IIIA*期非小细胞肺癌患者的辅助治疗。 *国际抗癌联盟/美国癌症联合会分期系统第 7 版转移性非小细胞肺癌 本品用于经国家药品监督管理局批准的检测方法评估为≥50%肿瘤细胞PD-L1染色阳性(TC≥50%)或肿瘤浸润PD-L1阳性免疫细胞(IC)覆盖≥10%的肿瘤面积(IC ≥10%)的表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性的转移性非小细胞肺癌(NSCLC)一线单药治疗。 该适应症是基于IMpower110临床研究中PD-L1高表达受试者的分析结果给予的附条件批准。该适应症的完全批准将取决于 ML42606 试验证实本品在中国人群的临床获益(见【临床试验】)。 本品联合培美曲塞和铂类化疗用于表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性的转移性非鳞状非小细胞肺癌(NSCLC)患者的一线治疗。 |
||||||
|
55 |
埃纳妥单抗注射液 |
Pfizer Inc. |
治疗用生物制品 |
3.1 |
本品单药适用于既往至少接受过三线治疗(包括一种蛋白酶体抑制剂、一种免疫调节剂和一种抗CD38单克隆抗体)的复发或难治性多发性骨髓瘤成人患者。 |
首次批准上市 |
|
56 |
艾沙妥昔 单抗注射液 |
Sanofi WinthropIndustrie |
治疗用生物制品 |
3.1 |
本品与泊马度胺和地塞米松联合用药,治疗既往接受过至少一线治疗(包括来那度胺和蛋白酶体抑制剂)的多发性骨髓瘤成人患者。 |
首次批准上市 |
|
序号 |
药品名称 |
上市许可持有人 |
药品类型 |
注册分类 |
适应症 |
首次批准上 市/增加适应 症 |
|
57 |
奥瑞利珠 单抗注射液 |
Roche Pharma (Schweiz) AG |
治疗用生物制品 |
3.1 |
本品适用于治疗: 成人复发型多发性硬化(RMS),包括临床孤立综合征、复发缓解型多发性硬化和活动性继发进展型多发性硬化; 成人原发进展型多发性硬化(PPMS)。 |
首次批准上市 |
|
58 |
布西珠单 抗注射液 |
NovartisPharma SchweizAG |
治疗用生物制品 |
3.1 |
用于治疗糖尿病黄斑水肿(DME)。 |
首次批准上市 |
|
59 |
利生奇珠 单抗注射液 |
AbbVie Inc. |
治疗用生物制品 |
3.1 |
本品适用于治疗对传统治疗或生物制剂治疗应答不足、失应答或不耐受的中重度活动性克罗恩病成年患者。 |
首次批准上市 |
|
60 |
利生奇珠 单抗注射 液(皮下注射) |
AbbVie Inc. |
治疗用生物制品 |
3.1 |
本品适用于治疗对传统治疗或生物制剂治疗应答不足、失应答或不耐受的中重度活动性克罗恩病成年患者。 |
首次批准上市 |
|
61 |
罗莫索珠 单抗注射液 |
Amgen Inc. |
治疗用生物制品 |
3.1 |
本品适用于骨折高风险的绝经后妇女的骨质疏松症。 |
首次批准上市 |
|
62 |
罗泽利昔 珠单抗注射液 |
UCB PharmaS.A. |
治疗用生物制品 |
3.1 |
与常规治疗药物联合用于治疗乙酰胆碱受体(AChR)或肌肉特异性受体酪氨酸激酶(MuSK)抗体阳性的成人全身型重症肌无力(gMG)患者。 |
首次批准上市 |
|
63 |
帕西生长 激素注射液 |
Somapacitan Injection |
治疗用生物制品 |
3.1 |
本品适用于因内源性生长激素分泌不足所致生长迟缓的2.5岁及以上儿童患者。 |
首次批准上市 |
|
序号 |
药品名称 |
上市许可持有人 |
药品类型 |
注册分类 |
适应症 |
首次批准上 市/增加适应 症 |
|
64 |
塔奎妥单抗注射液 |
Janssen-CilagInternational NV |
治疗用生物制品 |
3.1 |
本品单药适用于既往接受过至少三线治疗(包括一种蛋白酶体抑制剂、一种免疫调节剂和一种抗CD38 抗体)的复发或难治性多发性骨髓瘤成人患者。 |
首次批准上市 |
|
65 |
替利珠单 抗注射液 |
Provention Bio, Inc. |
治疗用生物制品 |
3.1 |
本品适用于8岁(含)以上儿童和成人1型糖尿病2 期患者,以延缓向1型糖尿病3期进展 |
首次批准上市 |
|
66 |
注射用卡 拉西珠单抗 |
Ablynx NV |
治疗用生物制品 |
3.1 |
本品适用于与血浆置换和免疫抑制疗法联合治疗获得性血栓性血小板减少性紫癜(aTTP)(也称为免疫介导的血栓性血小板减少性紫癜(iTTP))的成人和12岁及以上体重至少40 kg的青少年患者。 |
首次批准上市 |
|
67 |
注射用索特西普 |
Merck Sharp&Dohme LLC |
治疗用生物制品 |
3.1 |
适用于治疗 WHO 功能分级(FC)Ⅱ -Ⅲ级的肺动脉高压 (PAH, WHO第 1 组)成年患者,以改善患者的运动能力和WHO功能分级 |
首次批准上市 |
|
68 |
注射用坦昔妥单抗 |
Incyte BiosciencesDistribution B.V. |
治疗用生物制品 |
3.1 |
本品联合来那度胺适用于治疗复发或难治性且不适合自体干细胞移植(ASCT)的弥漫性大B细胞淋巴瘤(DLBCL)的成人患 者。 |
首次批准上市 |
|
69 |
本瑞利珠 单抗注射液 |
AstraZeneca AB |
治疗用生物制品 |
3.1 |
本品用于成人和 12 岁及以上青少年重度嗜酸粒细胞性哮喘(SEA)的维持治疗。用于成人嗜酸性肉芽肿性多血管炎 (EGPA)的治疗。 |
首次批准上 市、增加适应症 |
|
70 |
瑞利珠单抗注射液 |
Alexion EuropeSAS |
治疗用生物制品 |
3.1 |
全身型重症肌无力(gMG) 本品与常规治疗药物联合用于治疗抗乙酰胆碱受体(AChR)抗体阳性的成人全身型重症肌无力(gMG)患者。 视神经脊髓炎谱系疾病(NMOSD) |
首次批准上 市、增加适应症 |
|
序号 |
药品名称 |
上市许可持有人 |
药品类型 |
注册分类 |
适应症 |
首次批准上 市/增加适应 症 |
|
本品适用于治疗抗水通道蛋白4(AQP4)抗体阳性的成人视神经脊髓炎谱系疾病(NMOSD)患者。 |
||||||
|
71 |
纳武利尤 单抗注射液 |
Bristol-Myers Squibb Pharma EEIG |
治疗用生物制品 |
3.1 |
本品联合伊匹木单抗适用于由国家药品监督管理局批准的检测评估为PD-L1肿瘤比例分数(TPS)≥1%的表皮生长因子受体 (EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性的转移性非小细胞肺癌一线治疗。 |
增加适应症 |
|
72 |
帕博利珠 单抗注射 液 |
Merck Sharp&Dohme LLC |
治疗用生物制品 |
3.1 |
帕博利珠单抗联合注射用维恩妥尤单抗用于局部晚期或转移性尿路上皮癌成人患者。帕博利珠单抗单药用于通过充分验证的检测评估肿瘤表达PD-L1(综合阳性评分(CPS)≥1)的转移性或不可切除的复发性头颈部鳞状细胞癌(HNSCC)患者的一线治疗。 |
增加适应症 |
|
73 |
司库奇尤 单抗注射液 |
NovartisPharma SchweizAG |
治疗用生物制品 |
3.1 |
本品用于治疗中重度化脓性汗腺炎(反常性痤疮)的成人患者。 |
增加适应症 |
|
74 |
司美格鲁肽注射液 |
NovoNordiskA/S |
治疗用生物制品 |
3.1 |
适用于降低已确诊为心血管疾病且BMI≥27kg/m2成人患者的主要心血管不良事件(心血管死亡、非致死性心肌梗死、非致死性卒中)的风险 |
增加适应症 |
|
75 |
西妥昔单 抗注射液 |
Merck Europe B.V. |
治疗用生物制品 |
3.1 |
本品用于与恩考芬尼联合治疗既往接受过全身治疗的BRAFV600E突变型转移性结直肠癌成人患者。 |
增加适应症 |
|
76 |
伊匹木单抗注射液 |
Bristol-Myers Squibb Pharma EEIG |
治疗用生物制品 |
3.1 |
本品联合纳武利尤单抗适用于由国家药品监督管理局批准的检测评估为PD-L1肿瘤比例分数(TPS)≥1%的表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性的转移性非小细胞肺癌一线治疗。 |
增加适应症 |
|
序号 |
药品名称 |
上市许可持有人 |
药品类型 |
注册分类 |
适应症 |
首次批准上 市/增加适应 症 |
|
77 |
注射用德 曲妥珠单抗 |
DaiichiSankyoEurope GmbH |
治疗用生物制品 |
3.1 |
本品单药适用于治疗既往在转移性疾病阶段经一种或一种以上内分泌治疗进展的,不可切除或转移性激素受体(HR)阳性 HER2 低表达(IHC1+或IHC 2+/ISH-)或HER2 超低表达(IHC 0,存在细胞膜染色)成人乳腺癌患者。 |
增加适应症 |
|
78 |
注射用戈 沙妥珠单抗 |
GileadSciences, Inc. |
治疗用生物制品 |
3.1 |
本品用于治疗既往接受过内分泌治疗且在转移性疾病阶段接受过至少2 种其他系统性治疗的不可切除局部晚期或转移性的激素受体(HR)阳性、人类表皮生长因子受体2(HER2)阴性(IHC0、IHC1+或IHC 2+/ISH-)乳腺癌成人患者。 |
增加适应症 |
|
79 |
注射用罗特西普 |
Celgene Corporation,a Bristol-Myers Squibb Company |
治疗用生物制品 |
3.1 |
用于治疗极低危、低危和中危骨髓增生异常综合征引起的贫血且需要定期输注红细胞的成人患者。 |
增加适应症 |
|
80 |
注射用维 恩妥尤单抗 |
Astellas PharmaEurope B.V. |
治疗用生物制品 |
3.1 |
本品联合帕博利珠单抗用于局部晚期或转移性尿路上皮癌成人患者。 |
增加适应症 |
附件5 2025 年国家药监局批准的药品纳入加快上市程序情况
2025 年国家药监局批准的药品纳入加快上市程序情况
|
序号 |
药品名称 |
上市许可持有人 |
首次批准上市/增加适 应症 |
突破性治疗药物程序 |
附条件批准程序 |
优先审评审批程序 |
|
1 |
ω-3鱼油脂肪乳注射液 |
费森尤斯卡比华瑞制药有限公司 |
首次批准上市 |
√ |
||
|
2 |
阿夫凯泰片 |
Cytokinetics, Incorporated |
首次批准上市 |
√ |
√ |
|
|
3 |
埃纳妥单抗注射液 |
Pfizer Inc. |
首次批准上市 |
√ |
√ |
|
|
4 |
艾米迈托赛注射液 |
铂生卓越生物科技(北京)有限公司 |
首次批准上市 |
√ |
√ |
|
|
5 |
奥格特韦钠胶囊 |
浙江艾森药业有限公司 |
首次批准上市 |
√ |
||
|
6 |
巴氯芬口服溶液 |
成都倍特得诺药业有限公司 |
首次批准上市 |
√ |
||
|
7 |
波哌达可基注射液 |
上海信致医药科技有限公司 |
首次批准上市 |
√ |
√ |
|
|
8 |
菖麻熄风颗粒 |
黑龙江省济仁药业有限公司 |
首次批准上市 |
√ |
||
|
9 |
醋酸来法莫林片 |
住友制药(苏州)有限公司 |
首次批准上市 |
√ |
||
|
10 |
醋酸来法莫林注射用浓溶液 |
住友制药(苏州)有限公司 |
首次批准上市 |
√ |
||
|
11 |
厄贝沙坦氢氯噻嗪片 |
赛诺菲(杭州) 制药有限公司 |
首次批准上市 |
√ |
||
|
12 |
复方磺胺甲噁唑注射液 |
华夏生生药业(北京) 有限公司 |
首次批准上市 |
√ |
|
序号 |
药品名称 |
上市许可持有人 |
首次批准上市/增加适 应症 |
突破性治疗药物程序 |
附条件批准程序 |
优先审评审批程序 |
|
13 |
复方氯丝右哌甲酯胶囊 |
Commave Therapeutics SA |
首次批准上市 |
√ |
||
|
14 |
富马酸伏诺拉生片 |
天津武田药品有限公司 |
首次批准上市 |
√ |
||
|
15 |
枸橼酸戈来雷塞片 |
上海艾力斯医药科技股份有限公司 |
首次批准上市 |
√ |
√ |
√ |
|
16 |
古塞奇尤单抗注射液(静脉 输注) |
Janssen-Cilag International NV |
首次批准上市 |
√ |
√ |
|
|
17 |
九价人乳头瘤病毒疫苗(大 肠埃希菌) |
厦门万泰沧海生物技术有限公司 |
首次批准上市 |
√ |
||
|
18 |
口服六价重配轮状病毒减毒 活疫苗(Vero细胞) |
武汉生物制品研究所有限责任公司 |
首次批准上市 |
√ |
||
|
19 |
来特莫韦片(聂) |
MerckSharp& DohmeLLC,asubsidiaryofMerck& Co.,Inc. |
首次批准上市 |
√ |
||
|
20 |
利伐沙班片 |
拜耳医药保健有限公司 |
首次批准上市 |
√ |
||
|
21 |
利沙托克拉片 |
苏州亚盛药业有限公司 |
首次批准上市 |
√ |
√ |
|
|
22 |
芦沃美替尼片 |
上海复星医药产业发展有限公司 |
首次批准上市 |
√ |
√ |
|
|
23 |
马来酸噻吗洛尔凝胶 |
北京梅尔森医药技术开发有限公司 |
首次批准上市 |
√ |
||
|
24 |
吗替麦考酚酯干混悬剂 |
杭州中美华东制药有限公司 |
首次批准上市 |
√ |
||
|
25 |
莫米司特片 |
赣州和美药业股份有限公司 |
首次批准上市 |
√ |
|
序号 |
药品名称 |
上市许可持有人 |
首次批准上市/增加适 应症 |
突破性治疗药物程序 |
附条件批准程序 |
优先审评审批程序 |
|
26 |
苹果酸法米替尼胶囊 |
江苏恒瑞医药股份有限公司 |
首次批准上市 |
√ |
√ |
|
|
27 |
普基奥仑赛注射液 |
重庆精准生物技术有限公司 |
首次批准上市 |
√ |
√ |
√ |
|
28 |
氢溴酸他泽司他片 |
Epizyme, Inc. |
首次批准上市 |
√ |
√ |
|
|
29 |
巯嘌呤片(II) |
华润双鹤药业股份有限公司 |
首次批准上市 |
√ |
||
|
30 |
瑞米布替尼片 |
Novartis PharmaSchweiz AG |
首次批准上市 |
√ |
||
|
31 |
塞来昔布胶囊 |
晖致制药(大连)有限公司 |
首次批准上市 |
√ |
||
|
32 |
肾上腺素注射液 |
武汉久安药物研究院有限公司 |
首次批准上市 |
√ |
||
|
33 |
肾上腺素注射液 |
成都诺和晟鸿生物制药有限公司 |
首次批准上市 |
√ |
||
|
34 |
斯泰度塔单抗注射液 |
珠海泰诺麦博制药股份有限公司 |
首次批准上市 |
√ |
√ |
|
|
35 |
四价人乳头瘤病毒疫苗(汉 逊酵母) |
成都生物制品研究所有限责任公司 |
首次批准上市 |
√ |
||
|
36 |
索托克拉片 |
百济神州(苏州)生物科技有限公司 |
首次批准上市 |
√ |
√ |
|
|
37 |
塔奎妥单抗注射液 |
Janssen-Cilag International NV |
首次批准上市 |
√ |
√ |
√ |
|
38 |
替利珠单抗注射液 |
Provention Bio, Inc. |
首次批准上市 |
√ |
|
序号 |
药品名称 |
上市许可持有人 |
首次批准上市/增加适 应症 |
突破性治疗药物程序 |
附条件批准程序 |
优先审评审批程序 |
|
39 |
替妥尤单抗N01 注射液 |
信达生物制药(苏州) 有限公司 |
首次批准上市 |
√ |
||
|
40 |
褪黑素颗粒 |
Nobelpharma Co., Ltd. |
首次批准上市 |
√ |
||
|
41 |
托吡酯口服溶液 |
海南斯达制药有限公司 |
首次批准上市 |
√ |
||
|
42 |
维生素K₁注射液 |
海南倍特药业有限公司 |
首次批准上市 |
√ |
||
|
43 |
维生素K₁注射液 |
合肥亿帆生物制药有限公司 |
首次批准上市 |
√ |
||
|
44 |
小儿黄金止咳颗粒 |
北京东方运嘉药业有限公司 |
首次批准上市 |
√ |
||
|
45 |
盐酸阿曲生坦片 |
Novartis PharmaSchweiz AG |
首次批准上市 |
√ |
√ |
|
|
46 |
盐酸胍法辛缓释片 |
四川百利药业有限责任公司 |
首次批准上市 |
√ |
||
|
47 |
盐酸匹米替尼胶囊 |
默克雪兰诺(北京)医药有限公司 |
首次批准上市 |
√ |
√ |
|
|
48 |
盐酸依匹斯汀滴眼液 |
润尔眼科药物(广州) 有限公司 |
首次批准上市 |
√ |
||
|
49 |
盐酸右哌甲酯缓释胶囊 |
河南中帅药业有限公司 |
首次批准上市 |
√ |
||
|
50 |
伊那利塞片 |
Roche Pharma (Schweiz) AG |
首次批准上市 |
√ |
√ |
|
|
51 |
伊匹木单抗N01 注射液 |
信达生物医药科技(杭州)有限公司 |
首次批准上市 |
√ |
√ |
√ |
|
序号 |
药品名称 |
上市许可持有人 |
首次批准上市/增加适 应症 |
突破性治疗药物程序 |
附条件批准程序 |
优先审评审批程序 |
|
52 |
泽美妥司他片 |
江苏恒瑞医药股份有限公司 |
首次批准上市 |
√ |
√ |
√ |
|
53 |
重组人白蛋白注射液(水 稻) |
武汉禾元生物科技股份有限公司 |
首次批准上市 |
√ |
||
|
54 |
注射用镓[68Ga]戈泽肽药盒 |
Novartis PharmaSchweiz AG |
首次批准上市 |
√ |
||
|
55 |
注射用卡拉西珠单抗 |
Ablynx NV |
首次批准上市 |
√ |
||
|
56 |
注射用瑞康曲妥珠单抗 |
苏州盛迪亚生物医药有限公司 |
首次批准上市 |
√ |
√ |
√ |
|
57 |
注射用双羟萘酸帕瑞肽微球 |
Recordati Rare Diseases |
首次批准上市 |
√ |
||
|
58 |
注射用坦昔妥单抗 |
Incyte Biosciences Distribution B.V. |
首次批准上市 |
√ |
√ |
|
|
59 |
注射用头孢比罗酯钠 |
深圳华润九新药业有限公司 |
首次批准上市 |
√ |
||
|
60 |
注射用维贝柯妥塔单抗 |
乐普生物科技股份有限公司 |
首次批准上市 |
√ |
√ |
√ |
|
61 |
注射用维拉苷酶β |
北海康成(上海)生物科技有限公司 |
首次批准上市 |
√ |
||
|
62 |
注射用盐酸伊吡诺司他 |
广州必贝特医药股份有限公司 |
首次批准上市 |
√ |
√ |
√ |
|
63 |
注射用泽尼达妥单抗 |
百济神州(苏州)生物科技有限公司 |
首次批准上市 |
√ |
√ |
√ |
|
64 |
宗艾替尼片 |
Boehringer Ingelheim International GmbH |
首次批准上市 |
√ |
√ |
√ |
|
序号 |
药品名称 |
上市许可持有人 |
首次批准上市/增加适 应症 |
突破性治疗药物程序 |
附条件批准程序 |
优先审评审批程序 |
|
65 |
佐来曲替尼片 |
北京诺诚健华医药科技有限公司 |
首次批准上市 |
√ |
√ |
|
|
66 |
古塞奇尤单抗注射液 |
Janssen-Cilag International NV |
首次批准上市、增加适 应症 |
√ |
√ |
|
|
67 |
镥[¹了了Lu]特昔维匹肽注射液 |
Novartis PharmaSchweiz AG |
首次批准上市、增加适 应症 |
√ |
||
|
68 |
那米司特片 |
Boehringer Ingelheim International GmbH |
首次批准上市、增加适 应症 |
√ |
||
|
69 |
瑞普替尼胶囊 |
Bristol-Myers Squibb Company |
首次批准上市、增加适 应症 |
√ |
√ |
|
|
70 |
艾曲泊帕乙醇胺干混悬剂 |
山东则正医药技术有限公司 |
增加适应症 |
√ |
||
|
71 |
安瑞克芬注射液 |
海思科医药集团股份有限公司 |
增加适应症 |
√ |
||
|
72 |
奥德昔巴特胶囊 |
Ipsen Pharma |
增加适应症 |
√ |
||
|
73 |
伯瑞替尼肠溶胶囊 |
北京浦润奥生物科技有限责任公司 |
增加适应症 |
√ |
√ |
|
|
74 |
甲磺酸阿美替尼片 |
江苏豪森药业集团有限公司 |
增加适应症 |
√ |
√ |
|
|
75 |
赛沃替尼片 |
和记黄埔医药(上海) 有限公司 |
增加适应症 |
√ |
√ |
|
|
76 |
司普奇拜单抗注射液 |
成都康诺行生物医药科技有限公司 |
增加适应症 |
√ |
||
|
77 |
乌帕替尼缓释片 |
AbbVie Deutschland GmbH &Co.KG |
增加适应症 |
√ |
|
序号 |
药品名称 |
上市许可持有人 |
首次批准上市/增加适 应症 |
突破性治疗药物程序 |
附条件批准程序 |
优先审评审批程序 |
|
78 |
信迪利单抗注射液 |
信达生物制药(苏州) 有限公司 |
增加适应症 |
√ |
√ |
√ |
|
79 |
盐酸伊普可泮胶囊 |
Novartis PharmaSchweiz AG |
增加适应症 |
√ |
√ |
√ |
|
80 |
伊奈利珠单抗注射液 |
Horizon Therapeutics Ireland DAC |
增加适应症 |
√ |
||
|
81 |
依沃西单抗注射液 |
康方赛诺医药有限公司 |
增加适应症 |
√ |
√ |
|
|
82 |
注射用卡瑞利珠单抗 |
苏州盛迪亚生物医药有限公司 |
增加适应症 |
√ |
||
|
83 |
注射用芦康沙妥珠单抗 |
四川科伦博泰生物医药股份有限公司 |
增加适应症 |
√ |
√ |
√ |
|
84 |
注射用泰它西普 |
荣昌生物制药(烟台) 股份有限公司 |
增加适应症 |
√ |
√ |
|
|
85 |
注射用维迪西妥单抗 |
荣昌生物制药(烟台) 股份有限公司 |
增加适应症 |
√ |
√ |
附件6 2025 年纳入突破性治疗药物程序的药物
2025 年纳入突破性治疗药物程序的药物
|
序号 |
药品名称 |
适应症 |
|
1 |
注射用BL-B01D1 |
既往经含铂化疗及抗PD-1/PD-L1单抗治疗失败的复发性小细胞肺癌患者 |
|
2 |
SYS6010 |
经EGFR-TKI和含铂化疗治疗失败的EGFR突变阳性晚期非小细胞肺癌 |
|
3 |
瑞基奥仑赛注射液 |
一线治疗失败后不适合高剂量化疗和自体干细胞移植的成人复发或难治性大 B 细胞淋巴瘤 |
|
4 |
ZM-H1505R片 |
慢性乙型肝炎 |
|
5 |
注射用YL201 |
既往经PD-(L)1抑制剂和至少二线化疗治疗失败的复发或转移性鼻咽癌 |
|
6 |
IBI343 |
至少接受过一种系统性治疗的Claudin(CLDN)18.2 表达阳性的晚期胰腺导管腺癌 |
|
7 |
9MW2821 |
联合特瑞普利单抗用于治疗既往未经系统治疗的、不可手术切除的局部晚期或转移性尿路上皮癌 |
|
8 |
CG0070注射液 |
卡介苗(BCG)无应答的高危非肌层浸润性膀胱癌(NMIBC)伴原位癌(CIS)患者 |
|
9 |
ACT001胶囊 |
经过一线治疗或一线治疗中出现脑部新发病灶或原脑转移病灶进展的小细胞肺癌(smallcelllungcancer,SCLC)脑转移患者 |
|
10 |
M108 单抗注射液 |
本品联合吉西他滨+白蛋白结合型紫杉醇,用于局灶晚期不可切除或转移性的CLDN18.2阳性的胰腺癌患者的一线治疗 |
|
11 |
LM-108注射液 |
经免疫检查点抑制剂(ICI)治疗后疾病进展的微卫星高度不稳定(MSI-H)或错配修复缺陷(dMMR)晚期实体瘤患者 |
|
12 |
氟非尼酮胶囊 |
慢性乙型肝炎肝纤维化/肝硬化 |
|
序号 |
药品名称 |
适应症 |
|
13 |
注射用HS-20093 |
用于治疗经至少二线治疗后进展的骨肉瘤患者 |
|
14 |
注射用西罗莫司(白蛋白结合型) |
恶性血管周围上皮样细胞瘤 |
|
15 |
CT041自体CART细胞注射液 |
既往接受过至少二线治疗失败的Claudin18.2(CLDN18.2)表达阳性的晚期胃/食管胃结合部(G/GEJ)腺癌 |
|
16 |
奥雷巴替尼片 |
奥雷巴替尼联合化疗一线治疗新诊断费城染色体阳性急性淋巴细胞白血病(Ph+ ALL) |
|
17 |
注射用JSKN003 |
注射用JSKN003 用于治疗铂耐药复发性上皮性卵巢癌、原发性腹膜癌或输卵管癌。 |
|
18 |
注射用SHR-A1811 |
既往接受含铂化疗及免疫检查点抑制剂治疗失败的HER2 表达(IHC≥1+)的复发或转移性宫颈癌 |
|
19 |
IBI363 |
既往未经过系统性治疗的不可切除局部晚期或转移性肢端型及黏膜型恶性黑色素瘤 |
|
20 |
HRS-5965胶囊 |
原发性IgA肾病 |
|
21 |
SSGJ-707注射液 |
SSGJ-707一线治疗PD-L1 表达阳性的局部晚期或转移性非小细胞肺癌(NSCLC) |
|
22 |
注射用HS-20093 |
既往经过含铂化疗后进展或复发的驱动基因阴性的局部晚期或转移性非鳞状非小细胞肺癌 |
|
23 |
AK109注射液 |
AK109 联合AK104 用于治疗经含PD-(L)1 抑制剂治疗后进展的晚期鳞状非小细胞肺癌 |
|
24 |
PLB1004胶囊 |
适用于治疗既往接受EGFR-TKI治疗失败后,具有表皮生长因子受体(EGFR)突变、间质-上皮转化因子(MET)扩增和/或过表达的局部晚期或转移性非小细胞肺癌(NSCLC)的患者 |
|
25 |
GS1191-0445注射液 |
先天性凝血因子VIII缺乏引起的血友病A |
|
26 |
注射用HS-20089 |
铂耐药复发上皮性卵巢癌、输卵管癌或原发性腹膜癌患者 |
|
序号 |
药品名称 |
适应症 |
|
27 |
INS018_055片 |
特发性肺纤维化 |
|
28 |
FCN-159片 |
儿童朗格汉斯组织细胞增生症(Langerhanscellhistiocytosis,LCH) |
|
29 |
ICP-248片 |
既往接受过免疫化疗和布鲁顿氏酪氨酸激酶抑制剂(BTKi)治疗的复发/难治性套细胞淋巴瘤(r/rMCL)患者 |
|
30 |
注射用XNW27011 |
XNW27011 用于CLDN18.2 表达的局部晚期不可切除或转移性HER2阴性胃或胃食管结合部腺癌的三线及以上治疗。 |
|
31 |
ABSK-011胶囊 |
经免疫检查点抑制剂(ICI)和多靶点酪氨酸激酶抑制剂(mTKI)治疗的成纤维细胞生长因子19(FGF19)过表达的晚期肝细胞癌(HCC) |
|
32 |
XNW5004片 |
XNW5004拟用于治疗既往接受过至少3线全身系统治疗的复发或难治性滤泡性淋巴瘤(EZH2野生型)。 |
|
33 |
重组人源化抗表皮生长因子受体单克隆抗体注射液 |
JMT101联合伊立替康用于治疗二线或以上标准治疗失败的 RAS、RAF、EGFRECD和PIK3CA20外显子均野生型晚期结直肠癌。 |
|
34 |
注射用XNW28012 |
既往接受过2线系统性治疗(以吉西他滨和以氟尿嘧啶为基础的化疗)失败的转移性胰腺癌。 |
|
35 |
IBI363 |
经含铂化疗及抗PD-1/PD-L1免疫治疗失败的局部晚期或转移性鳞状非小细胞肺癌 |
|
36 |
KL-A167注射液 |
KL-A167注射液联合注射用SKB264一线治疗驱动基因阴性的局部晚期或转移性非鳞状非小细胞肺癌。 |
|
37 |
注射用SKB264 |
注射用SKB264 联合KL-A167注射液一线治疗驱动基因阴性的局部晚期或转移性非鳞状非小细胞肺癌。 |
|
38 |
BW-20507 注射液 |
慢性乙型肝炎病毒感染 |
|
39 |
VVN461滴眼液 |
非感染性前葡萄膜炎(NIAU) |
|
40 |
TDI01混悬液 |
治疗既往经过2线不超过5线系统治疗的中重度慢性移植物抗宿主病(cGVHD)。 |
|
序号 |
药品名称 |
适应症 |
|
41 |
LY3473329片 |
用于治疗伴有Lp(a)水平升高且确诊心血管疾病或发生首次心血管事件风险升高的成人患者 |
|
42 |
SC0062胶囊 |
SC0062胶囊拟用于治疗伴有白蛋白尿的糖尿病肾脏病(DKD)。 |
|
43 |
FT-001注射液 |
RPE65 双等位基因变异相关视网膜变性 |
|
44 |
LM-108注射液 |
克非奇拜单抗注射液(LM-108)联合特瑞普利单抗拟申请治疗既往经一线标准治疗失败的 CCR8 阳性的晚期胃或胃食管结合部(G/GEJ)腺癌患者 |
|
45 |
IBI343 |
至少接受过两种系统性治疗的Claudin(CLDN)18.2 表达阳性的局部晚期或转移性胰腺癌 |
|
46 |
HT-101注射液 |
慢性乙型肝炎病毒感染 |
|
47 |
GST-HG131片 |
本品拟用于慢性乙型肝炎(HBV)的治疗。 |
|
48 |
注射用TQB2102 |
本品拟用于HER2阳性早期或局部晚期乳腺癌患者的新辅助治疗 |
|
49 |
注射用ZG006 |
ZG006单药治疗既往经含铂化疗及至少1 种其它系统治疗后(三线及以上)复发或进展的晚期小细胞肺癌患者 |
|
50 |
注射用KJ103 |
抗肾小球基底膜(GBM)病 |
|
51 |
吸入用TQC3721混悬液 |
慢性阻塞性肺疾病(COPD)的维持治疗 |
|
52 |
TQ05105片 |
拟用于慢性移植物抗宿主病的治疗。 |
|
53 |
PA3-17注射液 |
成人复发/难治性T淋巴母细胞白血病/淋巴瘤(r/rT-ALL/LBL) |
|
54 |
阿得贝利单抗注射液 |
SHR-A1811 联合阿得贝利单抗用于PD-L1阳性(CPS≥1)局部复发不可切除或转移性三阴性乳腺癌的一线治疗 |
|
序号 |
药品名称 |
适应症 |
|
55 |
BI1810631片 |
用于携带HER2(ERBB2)酪氨酸激酶结构域(TKD)激活突变的不可切除或转移性非小细胞肺癌(NSCLC)成人患者的一线治疗 |
|
56 |
RC148注射液 |
RC148 联合多西他赛治疗经PD-1/PD-L1 抑制剂和含铂化疗(联合或序贯)治疗失败的驱动基因阴性局部晚期或转移性非小细胞肺癌受试者。 |
|
57 |
注射用LM-302 |
注射用LM-302 联合抗特瑞普利单抗一线治疗Claudin18.2阳性的局部晚期或转移性胃及胃食管交界部腺癌 |
|
58 |
注射用ATG-022 ADC |
ATG-022拟用于治疗既往经过2线及以上治疗的Claudin 18.2阳性表达,HER2阴性的不可切除或转移性胃癌或胃食管结合部腺癌(GC/GEJ)。 |
|
59 |
MRG004A |
既往经至少二线系统性治疗失败的晚期胰腺癌 |
|
60 |
IN10018片 |
IN10018 联合D-1553治疗至少经过二线治疗的KRASG12C突变阳性的局晚期或转移性结直肠癌(CRC) |
|
61 |
赫基仑赛注射液 |
儿童复发或难治性B细胞急性淋巴细胞白血病(r/rB-ALL) |
|
62 |
注射用BL-B01D1 |
铂耐药复发上皮性卵巢癌、输卵管癌或原发性腹膜癌患者 |
|
63 |
RY_SW01细胞注射液 |
系统性硬化症 |
|
64 |
HT-102注射液 |
HT-102注射液与HT-101注射液联合使用,治疗慢性乙型肝炎病毒感染 |
|
65 |
人干扰素α1b吸入溶液 |
小儿呼吸道合胞病毒性下呼吸道感染(肺炎、毛细支气管炎) |
|
66 |
HRS-5635注射液 |
用于治疗慢性乙型肝炎 |
|
67 |
IBI354 |
既往经奥沙利铂、氟尿嘧啶类和伊立替康治疗失败的HER2 表达IHC2+或3+的结直肠癌 |
|
68 |
注射用SHR-1501 |
注射用SHR-1501 联合卡介苗(BCG)用于BCG无应答的原位癌(CIS)。 |
|
序号 |
药品名称 |
适应症 |
|
69 |
注射用BL-B01D1 |
既往经含铂化疗及PD-1/PD-L1 抑制剂治疗失败的不可手术切除的局部晚期或转移性尿路上皮癌患者 |
|
70 |
注射用MRG003 |
本品联合HX008(普特利单抗)注射液用于治疗既往至少经过铂类和PD-1/L1治疗失败的复发或转移性鼻咽癌 |
|
71 |
重组人源化抗PD-1 单克隆抗体注射液 |
本品联合注射用MRG003(注射用维贝柯妥塔单抗)用于治疗既往至少经过铂类和PD-1/L1治疗失败的复发或转移性鼻咽癌 |
|
72 |
DS-7300a |
IfinatamabDeruxtecan(I-DXd, DS-7300a)用于治疗在含铂化疗期间或之后出现疾病进展的广泛期小细胞肺癌成人患者。 |
|
73 |
注射用 TQB2102 |
拟用于既往经奥沙利铂、伊立替康、氟尿嘧啶类药物治疗失败的HER2 IHC3+晚期结直肠癌 |
|
74 |
ONC-392注射液 |
ONC-392 用于治疗经含PD-(L)1抑制剂治疗后进展的晚期鳞状非小细胞肺癌 |
|
75 |
AK112注射液 |
依沃西单抗联合化疗一线治疗局部晚期不可切除或转移性三阴性乳腺癌 |
|
76 |
注射用BL-M07D1 |
BL-M07D1拟选择目标人群为:既往经一线抗HER2治疗及一线标准化疗方案治疗失败的HER2阳性局部晚期或转移性胃或胃食管结合部腺癌患者 |
|
77 |
重组抗PD-1人源化单克隆抗体注射液 |
斯鲁利单抗注射液联合化疗新辅助/辅助治疗胃癌 (GCneo) |
|
78 |
JMKX001899片 |
既往经奥沙利铂、伊立替康和氟尿嘧啶类治疗失败的KRASG12C突变阳性的无法行根治性治疗的局部晚期或转移性结直肠癌患者。 |
|
79 |
氢溴酸氘瑞米德韦干混悬剂 |
治疗呼吸道合胞病毒感染 |
|
80 |
BI764198胶囊 |
治疗患有原发性局灶性节段性肾小球硬化症(FSGS)、体重至少为40 kg的成人和≥12岁青少年患者。 |
|
81 |
VGN-R09b |
芳香族L-氨基酸脱羧酶缺乏症(AADCD) |
|
82 |
注射用QLC5508 |
经初始含铂治疗失败的复发性小细胞肺癌(SCLC) |
|
序号 |
药品名称 |
适应症 |
|
83 |
注射用ZG006 |
ZG006单药治疗既往至少经含铂方案治疗后复发或进展(二线及以上)且DLL3阳性(≥50%的肿瘤细胞DLL3任意强度染色)的晚期神经内分泌癌患者 |
|
84 |
磷酸泊沃昔替尼片 |
本品用于成人患者非节段型白癜风的治疗。 |
|
85 |
JNJ-78278343注射液 |
用于治疗接受过雄激素受体(AR)通路抑制剂和紫杉烷类化疗治疗的转移性去势抵抗性前列腺癌(mCRPC)成人患者,对于携带乳腺癌基因(BRCA)1/2突变(胚系和/或体系)的患者,还应接受过一种聚腺苷二磷酸核糖聚合酶(PARP)抑制剂治疗。 |
|
86 |
注射用AMT-253 |
既往经一线治疗的不可手术的局部晚期、复发或转移性黑色素瘤 |
|
87 |
TJ004309注射液 |
不可手术切除的局部晚期或转移性PD-L1阳性和CD73高表达非小细胞肺癌(NSCLC)的一线治疗 |
|
88 |
注射用SHR-A1904 |
既往至少一线标准治疗失败或不能耐受的(Claudin18.2)CLDN18.2阳性晚期胃癌或胃食管结合部腺癌患者 |
|
89 |
NB003片 |
胃肠道间质瘤的三线治疗 |
附件7 2025 年国家药监局附条件批准的药品
2025 年国家药监局附条件批准的药品
|
序号 |
药品通用名称 |
药品上市许可持有人 |
附条件批准适应症 |
首次批准上市/增加适应症 |
|
1 |
艾米迈托赛注射液 |
铂生卓越生物科技(北京)有限公司 |
本品用于治疗 14 岁以上消化道受累为主的激素治疗失败的急性移植物抗宿主病(aGVHD) |
首次批准上市 |
|
2 |
塔奎妥单抗注射液 |
Janssen-CilagInternational NV |
本品单药适用于既往接受过至少三线治疗(包括一种蛋白酶体抑制剂、一种免疫调节剂和一种抗CD38 抗体)的复发或难治性多发性骨髓瘤成人患者。 |
首次批准上市 |
|
3 |
埃纳妥单抗注射液 |
Pfizer Inc. |
本品单药适用于既往至少接受过三线治疗(包括一种蛋白酶体抑制剂、一种免疫调节剂和一种抗 CD38单克隆抗体)的复发或难治性多发性骨髓瘤成人患者。 |
首次批准上市 |
|
4 |
氢溴酸他泽司他片 |
Epizyme, Inc. |
本品单药用于既往接受过至少两种系统性治疗后的EZH2突变阳性复发或难治性滤泡性淋巴瘤 (FL) 成人患者。 |
首次批准上市 |
|
5 |
注射用坦昔妥单抗 |
Incyte BiosciencesDistribution B.V. |
本品联合来那度胺适用于治疗复发或难治性且不适合自体干细胞移植(ASCT)的弥漫性大B 细胞淋巴瘤(DLBCL)的成人患者 |
首次批准上市 |
|
6 |
枸橼酸戈来雷塞片 |
上海艾力斯医药科技股份有限公司 |
本品适用于至少接受过一种系统性治疗的鼠类肉瘤病毒癌基因(KRAS)G12C突变型的晚期非小细胞肺癌(NSCLC)成人患者。 |
首次批准上市 |
|
7 |
注射用瑞康曲妥珠单抗 |
苏州盛迪亚生物医药有限公司 |
本品单药适用于治疗存在 HER2(ERBB2)激活突变且既往接受过至少一种系统治疗的不可切除的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。 |
首次批准上市 |
|
8 |
注射用泽尼达妥单抗 |
百济神州(苏州)生物科技有限公司 |
本品用于既往接受过全身治疗的 HER2高表达(IHC3+)的不可切除局部晚期或转移性胆道癌患者。 |
首次批准上市 |
|
9 |
注射用盐酸伊吡诺司他 |
广州必贝特医药股份有限公司 |
本品单药适用于既往接受过至少两线系统性治疗的复发或难治性弥漫性大 B细胞淋巴瘤成人患者。 |
首次批准上市 |
|
序号 |
药品通用名称 |
药品上市许可持有人 |
附条件批准适应症 |
首次批准上市/增加适应症 |
|
10 |
利沙托克拉片 |
苏州亚盛药业有限公 司 |
本品适用于既往经过至少包含布鲁顿酪氨酸激酶(BTK)抑制剂在内的一种系统治疗的成人慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)患者。 |
首次批准上市 |
|
11 |
宗艾替尼片 |
Boehringer IngelheimInternational GmbH |
本品单药适用于治疗存在 HER2(ERBB2)激活突变且既往接受过至少一种系统治疗的不可切除的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。 |
首次批准上市 |
|
12 |
泽美妥司他片 |
江苏恒瑞医药股份有限公司 |
本品用于既往接受过至少1线系统性治疗的复发或难治外周T细胞淋巴瘤成人患者。 |
首次批准上市 |
|
13 |
盐酸阿曲生坦片 |
NovartisPharma SchweizAG |
本品适用于降低有疾病快速进展风险的原发性免疫球蛋白A肾病(IgA肾病)成人患者的蛋白尿。 |
首次批准上市 |
|
14 |
注射用维贝柯妥塔单抗 |
乐普生物科技股份有限公司 |
本品用于既往经至少二线系统化疗和PD-1/PD-L1抑制剂治疗失败的复发/转移性鼻咽癌成人患者 |
首次批准上市 |
|
15 |
普基奥仑赛注射液 |
重庆精准生物技术有限公司 |
本品用于治疗3~21岁CD19阳性的难治或复发(首次缓解12 个月后复发需经挽救化疗)的急性B 淋巴细胞白血病患者。 |
首次批准上市 |
|
16 |
奥格特韦钠胶囊 |
浙江艾森药业有限公 司 |
本品用于治疗轻中型新型冠状病毒感染(COVID-19)的成年患者。 |
首次批准上市 |
|
17 |
佐来曲替尼片 |
北京诺诚健华医药科技有限公司 |
本品适用于符合下列条件的成人和12岁以上青少年实体瘤患者,经充分验证的检测方法诊断为携带神经营养酪氨酸受体激酶(NTRK)融合基因且不包括已知获得性耐药突变,患有局部晚期、转移性疾病或手术切除可能导致严重并发症的患者,以及无满意替代治疗或既往治疗失败的患者。 |
首次批准上市 |
|
18 |
索托克拉片 |
百济神州(苏州)生物科技有限公司 |
本品适用于既往经过至少包含布鲁顿酪氨酸激酶(BTK)抑制剂在内的一种系统治疗的成人慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)患者。 |
首次批准上市 |
|
序号 |
药品通用名称 |
药品上市许可持有人 |
附条件批准适应症 |
首次批准上市/增加适应症 |
|
19 |
索托克拉片 |
百济神州(苏州)生物科技有限公司 |
本品适用于既往接受过至少两种系统性治疗(含布鲁顿氏酪氨酸激酶[BTK]抑制剂)的复发或难治性套细胞淋巴瘤(MCL)成人患者。 |
首次批准上市 |
|
20 |
伊匹木单抗N01注射液 |
信达生物医药科技(杭州)有限公司 |
本品联合信迪利单抗用于可手术切除的IIB-III 期微卫星高度不稳定型(MSI-H)或错配修复缺陷型(dMMR)结肠癌患者的新辅助治疗。 |
首次批准上市 |
|
信迪利单抗注射液 |
信达生物制药(苏州)有限公司 |
本品联合伊匹木单抗 N01用于可手术切除的 IIB-III期微卫星高度不稳定型(MSI-H)或错配修复缺陷型(dMMR)结肠癌患者的新辅助治疗 |
增加适应症 |
|
|
21 |
苹果酸法米替尼胶囊 |
江苏恒瑞医药股份有限公司 |
本品联合注射用卡瑞利珠单抗用于既往接受含铂化疗治疗失败但未接受过贝伐珠单抗治疗的复发或转移性宫颈癌患者。 |
首次批准上市 |
|
注射用卡瑞利珠单抗 |
苏州盛迪亚生物医药有限公司 |
本品联合苹果酸法米替尼用于既往接受含铂化疗治疗失败但未接受过贝伐珠单抗治疗的复发或转移性宫颈癌患者。 |
增加适应症 |
|
|
22 |
注射用芦康沙妥珠单抗 |
四川科伦博泰生物医药股份有限公司 |
本品用于经表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI)和含铂化疗治疗后进展的EGFR 基因突变阳性的局部晚期或转移性非鳞状非小细胞肺癌(NSCLC)成人患者的治疗。 |
增加适应症 |
|
23 |
盐酸伊普可泮胶囊 |
NovartisPharma SchweizAG |
本品用于降低有疾病快速进展风险的原发性免疫球蛋白A肾病(IgA肾病)成人患者的蛋白尿水平,一般来说,这类患者的尿蛋白肌酐比值(UPCR)≥≥CR 人患者的蛋。 |
增加适应症 |
|
24 |
伯瑞替尼肠溶胶囊 |
北京浦润奥生物科技有限责任公司 |
本品用于治疗具有间质-上皮转化因子(MET)扩增的局部晚期或转移性非小细胞肺癌患者。 |
增加适应症 |
附件8 2025 年药审中心发布的指导原则
2025 年药审中心发布的指导原则
|
序号 |
通告号 |
指导原则 |
发布时间 |
|
1 |
2025 年第55号 |
中药复方制剂新药研发人用经验收集整理技术指导原 则(试行) |
2025/12/30 |
|
2 |
2025 年第54号 |
单臂临床试验用于支持抗肿瘤药物常规上市申请技术 指导原则 |
2025/12/30 |
|
3 |
2025 年第53号 |
嗜酸性粒细胞性食管炎治疗药物临床试验技术指导原 则 |
2025/12/30 |
|
4 |
2025 年第52号 |
艾滋病免疫功能重建不全治疗药物临床试验技术指导 原则 |
2025/12/30 |
|
5 |
2025 年第51号 |
治疗慢性气道疾病的靶向炎症因子类生物制剂临床试 验技术指导原则(试行) |
2025/12/30 |
|
6 |
2025 年第50号 |
针对泛肿瘤的抗肿瘤药物临床研发技术指导原则 |
2025/12/30 |
|
7 |
2025 年第49号 |
疫苗临床试验不良事件分级标准指导原则(修订版) |
2025/12/5 |
|
8 |
2025 年第48号 |
多联疫苗临床试验技术指导原则 |
2025/11/18 |
|
9 |
2025 年第47号 |
重组糖蛋白激素类产品药学研究与评价技术指导原则 |
2025/11/10 |
|
10 |
2025 年第45号 |
创新药研发中涉及适老化设计时的一般原则及考虑要 点(试行) |
2025/10/29 |
|
11 |
2025 年第44号 |
老年人群参与创新药临床试验的关键要素及试验设计 要点(试行) |
2025/10/29 |
|
12 |
2025 年第43号 |
药品说明书中涉及老年人群用药信息的撰写要点(试 行) |
2025/10/29 |
|
13 |
2025 年第46号 |
化学药品批准后药学变更管理方案技术指导原则(试 行) |
2025/10/28 |
|
14 |
2025 年第42号 |
带状疱疹疫苗临床试验技术指导原则 |
2025/10/27 |
|
15 |
2025 年第39号 |
重组腺相关病毒载体类体内基因治疗产品申报上市药 学共性问题与技术要求 |
2025/9/18 |
|
16 |
2025 年第38号 |
创新药研发期间风险管理计划撰写技术指导原则(试 行) |
2025/9/12 |
|
17 |
2025 年第37号 |
重组胰高血糖素样肽-1受体激动剂药学研究与评价技 术指导原则(试行) |
2025/9/12 |
|
18 |
2025 年第31号 |
口服药物胃pH 依赖性药物相互作用评价技术指导原 则 |
2025/9/8 |
|
19 |
2025 年第34号 |
抗体偶联药物临床药理学研究技术指导原则 |
2025/9/8 |
|
20 |
2025 年第36号 |
疫苗佐剂非临床研究技术指导原则 |
2025/8/28 |
|
21 |
2025 年第33号 |
骨关节炎新药临床研发技术指导原则 |
2025/8/14 |
|
22 |
2025 年第29号 |
药物暴露-效应关系研究技术指导原则 |
2025/7/30 |
|
23 |
2025 年第28号 |
发酵或半合成化学仿制药抗生素有关物质限度制定指 导原则 |
2025/7/30 |
|
24 |
2025 年第26号 |
罕见疾病药物临床药理学研究技术指导原则 |
2025/7/30 |
|
25 |
2025 年第25号 |
模型引导的罕见疾病药物研发技术指导原则 |
2025/7/30 |
|
26 |
2025 年第30号 |
生物类似药药学相似性研究的问题与解答 |
2025/7/22 |
|
27 |
2025 年第27号 |
存在未满足临床需求的严重细菌感染性疾病抗菌药物 临床试验技术指导原则 |
2025/7/18 |
|
28 |
2025年第17号 |
化学药品口溶膜剂药学研究技术指导原则(试行) |
2025/7/18 |
|
29 |
2025 年第23号 |
抗HIV感染药物临床耐药性研究及数据递交指导原则 |
2025/7/2 |
|
30 |
2025 年第22号 |
局部起效化学仿制药体外释放(IVRT)与体外透皮 (IVPT)研究技术指导原则(试行) |
2025/6/20 |
|
31 |
2025 年第20号 |
已上市血液制品生产场地变更研究技术指导原则(试 行) |
2025/5/29 |
|
32 |
2025 年第21号 |
儿童药物临床试验安全信息评估与报告技术指导原则 (试行) |
2025/5/29 |
|
33 |
2025年第19号 |
阿尔茨海默病治疗药物临床试验技术指导原则(试 行) |
2025/5/22 |
|
34 |
2025年第16号 |
疫苗临床试验技术指导原则 |
2025/3/31 |
|
35 |
2025年第13号 |
晚期胃癌新药临床试验设计指导原则 |
2025/2/14 |
|
36 |
2025年第11号 |
地中海贫血基因治疗产品临床试验技术指导原则(试 行) |
2025/2/7 |
|
37 |
2025年第12号 |
生物类似药说明书撰写技术指导原则 |
2025/2/7 |
|
38 |
2025年第10号 |
患者报告结局指标用于风湿免疫性疾病临床试验的技 术指导原则 |
2025/2/7 |
|
39 |
2025年第9号 |
疫苗说明书临床相关信息撰写指导原则(试行) |
2025/1/23 |
|
40 |
2025年第8号 |
预防用猴痘疫苗药学研究技术指导原则(试行) |
2025/1/23 |
|
41 |
2025年第7号 |
预防用mRNA疫苗非临床研究技术指导原则 |
2025/1/23 |
|
42 |
2025年第6号 |
化药口服固体制剂中间产品存放时限研究技术指导原 则 |
2025/1/17 |
|
43 |
2025年第5号 |
放射性治疗药物申报上市临床风险管理计划技术指导 原则 |
2025/1/16 |
|
44 |
2025第4号 |
预防用猴痘疫苗非临床有效性研究技术指导原则(试 行) |
2025/1/10 |
|
45 |
2025年第3号 |
抗猴痘病毒药物临床试验技术指导原则(试行) |
2025/1/10 |
|
46 |
2025年第2号 |
治疗子宫内膜癌新药临床研发技术指导原则(试行) |
2025/1/9 |
|
47 |
2025年第1号 |
化学仿制药口服制剂经肠内营养管给药体外对比研究 技术指导原则 |
2025/1/9 |
|
48 |
2024 年第55号 |
抗体类药物临床药理学研究技术指导原则 |
2025/1/2 |
|
49 |
2024 年第55号 |
肽类药物临床药理学研究技术指导原则 |
2025/1/2 |
附件9 2025 年药审中心药审云课堂开展情况
2025 年药审中心药审云课堂开展情况
|
序号 |
培训时间 |
期数 |
培训内容 |
参加人数 |
|
1 |
2025年1月10 日 |
药审云课堂第一期 |
《治疗慢性心力衰竭药物临床试验技术指导原则》解读 |
10000 余人 |
|
《间充质干细胞防治移植物抗宿主病临床试验技术指导原 则(试行)》解读 |
||||
|
《基于药代动力学方法支持用于肿瘤治疗的抗PD-1PD-L1抗体可选给药方案的技术指导原则》解读 |
||||
|
《基于疾病登记的真实世界数据应用指导原则(试行)》 解读 |
||||
|
2 |
2025年2月14 日 |
药审云课堂第二期 |
中药PCMC 质量控制研究的考虑 |
9000 余人 |
|
中药新药工艺研究、过程控制及变更研究技术要求的一般 考虑 |
||||
|
化学创新药质量控制与常见问题分析 |
||||
|
生物类似药CMC 质量控制研究的考虑 |
||||
|
3 |
2025年3月7日 |
药审云课堂第三期 |
抗肿瘤药物剂量选择策略 |
11000 余人 |
|
抗肿瘤联合用药开发中的临床关注要点 |
||||
|
抗肿瘤药物临床研发策略回顾与考虑 |
|
序号 |
培训时间 |
期数 |
培训内容 |
参加人数 |
|
化学药品注册受理审查指南修订情况介绍 |
||||
|
生物制品注册受理审查指南修订情况介绍 |
||||
|
4 |
2025年4月11日 |
药审云课堂第四期 |
药物变更的总体考虑 |
11000 余人 |
|
化学药创新药临床试验期间药学变更研究技术要求和案例 分析 |
||||
|
生物制品临床期间变更相关非临床研究和评价关注点 |
||||
|
已上市境外生产生物制品转移至境内生产的生物制品上市 注册申请申报资料要求解读(治疗用生物制品) |
||||
|
已上市境外生产生物制品转移至境内生产的生物制品上市 注册申请申报资料要求解读(预防用生物制品) |
||||
|
5 |
2025年5月9日 |
药审云课堂第五期 |
《已上市化学药品药学变更研究技术指导原则(试行)》 中等变更解读 |
12000 余人 |
|
《化药口服固体制剂中间产品存放时限研究技术指导原 则》解读 |
||||
|
《化学仿制药口服制剂经肠内营养管给药体外对比研究技 术指导原则》解读 |
||||
|
高变异药物生物等效性研究常见问题 |
||||
|
窄治疗窗药物生物等效性研究常见问题 |
|
序号 |
培训时间 |
期数 |
培训内容 |
参加人数 |
|
6 |
2025年6月6日 |
药审云课堂第六期 |
药品注册受理程序、要求及常见问题 |
11000 余人 |
|
申请人在品种审评期间如何与CDE 做好互动沟通 |
||||
|
药品注册核查检验启动工作程序及常见问题分析 |
||||
|
创新药临床试验安全信息报告与评估要求及常见问题分析 |
||||
|
7 |
2025年7月4日 |
药审云课堂第七期 |
ICH 基本情况介绍 |
11000 余人 |
|
电子申报资料的机遇与挑战——eCTD |
||||
|
《E6(R3):药物临床试验质量管理规范(GCP)》基本框 架及新变化 |
||||
|
《E8(R1):临床研究的一般考虑》实施经验分享 |
||||
|
《E9(R1):临床试验中的估计目标与敏感性分析》实施情 况介绍 |
||||
|
8 |
2025年8月8 日 |
药审云课堂第八期 |
IND申报药学审评常见问题及案例分析 |
11000 余人 |
|
抗体偶联药物(ADC)药学研究的审评考虑 |
||||
|
IND非临床申报资料要求及常见问题分析 |
|
序号 |
培训时间 |
期数 |
培训内容 |
参加人数 |
|
IND申报临床资料要求及常见问题 |
||||
|
9 |
2025年9月5日 |
药审云课堂第九期 |
ICH《M4Q(R2):人用药品注册通用技术文档:质量》 指南修订进展简介 |
10000 余人 |
|
《化学药品仿制药上市许可申请模块二药学资料撰写要求 (原料药)(试行)》介绍及解读 |
||||
|
《化学药品仿制药上市许可申请模块二药学资料撰写要求 (制剂)(试行)》介绍及解读 |
||||
|
化学仿制药制剂研究常见问题和案例分析 |
||||
|
化学仿制药原料药研究常见问题和案例分析 |
||||
|
10 |
2025年10月17 日 |
药审云课堂第十期 |
创新药药学研究关键技术考虑 |
10000 余人 |
|
创新药药理毒理研究关键技术考虑 |
||||
|
重大慢病药物临床试验设计的特殊考虑 |
||||
|
抗肿瘤药物临床试验设计的特殊考虑 |
||||
|
创新药临床试验设计的一般技术考虑 |
||||
|
创新药监管框架及整体研发策略 |
|
序号 |
培训时间 |
期数 |
培训内容 |
参加人数 |
|
11 |
2025年11月7 日 |
药审云课堂第十一期 |
中药注册受理审查指南修订情况介绍 |
10000 余人 |
|
中药制剂稳定性研究技术要求 |
||||
|
已上市中药变更说明书中安全性内容的申报资料撰写要求 和审评考虑 |
||||
|
“三结合”注册审评证据体系下的中药新药研发 |
||||
|
12 |
2025年12月5 日 |
药审云课堂第十二期 |
创新药注册申请沟通交流及受理常见问题 |
10000 余人 |
|
治疗用生物制品关键问题考虑 |
||||
|
先进治疗药品临床审评中常见问题及相关考虑 |
||||
|
生物制品上市后变更研究的考虑及案例分析 |
||||
|
纳米药物审评相关要求 |

站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。
上一篇:近日,质子治疗系统获批上市,创新医疗器械已达421款!
下一篇:返回列表
ONE-STOP SERVICE
免费赠送3万家医疗器械企业名录