
发布时间:2021-01-21
附件:心电图机注册技术审查指导原则(2017年修订版).doc
本指导原则是对心电图机产品的一般要求,申请人应依据具体产品的特性对注册申报资料的内容进行充实和细化。申请人还应依据具体产品的特性确定其中的具体内容是否适用,若不适用,需具体阐述其理由及相应的科学依据。
本指导原则是对申请人和审查人员的指导性文件,但不包括注册审批所涉及的行政事项,亦不作为法规强制执行,如果有能够满足相关法规要求的其他方法,也可以采用,但是需要提供详细的研究资料和验证资料。应在遵循相关法规的前提下使用本指导原则。
本指导原则是在现行法规和标准体系以及当前认知水平下制定的,随着法规和标准的不断完善,以及科学技术的不断发展,本指导原则相关内容也将进行适时的调整。
一、适用范围
本指导原则适用于《医疗器械分类目录》(国药监械〔2002〕302号)中分类代号为6821的心电图机产品,管理类别为Ⅱ类。
二、技术审查要点
(一)产品名称的要求
产品的命名应符合国家关于医疗器械命名规则的要求,采用《医疗器械分类目录》(国药监械〔2002〕302号)或国家标准、行业标准中的通用名称,一般可以按“特征词+核心词”的方式命名,例如:单道心电图机、单道自动心电图机、多道心电图机、多道自动心电图机等。
产品名称不应加以型号、系列作为通用名称。
(二)产品的结构和组成
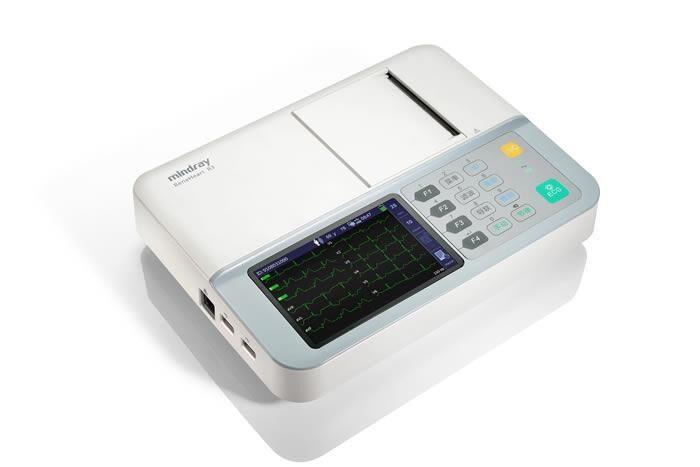
产品一般为台式或便携式,由主机、患者电缆和电极组成,电极分为可重复使用和一次性使用两种形式。记录方式可采用热笔式或热线阵记录方式等。某些产品带有信号输入或输出端口,以及可对心电图进行辅助分析的专用软件。
心电图机产品按产品应用部分的防电击程度可划分为:B型、BF型、CF型;
按功能可划分为:具有分析功能或不具有分析功能;
按记录形式可划分为:单道、多道;
按产品电源部分可分为:直流、交流或交直流两用;
按记录方式可划分为:热笔式打印、热阵式打印。
 width="454" />
width="454" />
1)单道心电图机,2)多道心电图机,3)患者电缆、电极,4)一次性使用心电电极。
(三)产品工作原理/作用机理
心电图机产品通过患者电缆联接体表放置的电极,测定心脏动作电位,生成供诊断用的心电图。
(四)注册单元划分的原则和实例
注册单元的划分应根据产品的预期用途、性能指标、结构组成进行综合判定,应考虑产品性能规格或设计规格、软件、电路、部件、材料、运行原理或实体布局等。具有同一种应用部分、同一种功能但电源部分和记录方式不同的产品可考虑作为同一注册单元。例如,交流BF型不具有分析功能的单道心电图机和交直流两用BF型不具有分析功能的单道心电图机可作同一注册单元。
(五)产品适用的相关标准
目前与心电图机产品相关的常用标准举例如下:
表1 相关产品标准
| GB 9706.1—2007 | 医用电气设备 第1部分:安全通用要求 |
| GB 10793—2000 | 医用电气设备 第2部分 心电图机安全专用要求 |
| GB/T 14710—2009 | 医用电器环境要求及试验方法 |
| GB/T 16886.1—2011 | 医疗器械生物学评价 第1部分:风险管理过程中的评价与试验 |
| GB/T 16886.5—2003 | 医疗器械生物学评价 第5部分:体外细胞毒性试验 |
| GB/T 16886.10—2005 | 医疗器械生物学评价 第10部分:刺激与迟发型超敏反应试验 |
| YY 0782—2010 | 医用电气设备 第2-51部分:记录和分析型单道和多道心电图机安全和基本性能专用要求 |
| YY 1139—2013 | 心电诊断设备 |
| YY 0505—2012 | 医用电气设备 第1-2部分:安全通用要求 并列标准:电磁兼容要求和试验 |
| YY/T 0196—2005 | 一次性使用心电电极 |
| YY/T 0316—2008 | 医疗器械 风险管理对医疗器械的应用 |
| YY/T 0708—2009 | 医用电气设备 第1-4部分:安全通用要求 并列标准:可编程医用电气系统 |
上述标准包括了产品技术要求中经常涉及的部件标准和方法标准。某些企业还会根据自身产品的特点引用一些行业外标准和较为特殊的标准。
产品适用标准的引用应注意以下两点:1)引用标准的齐全性和适用性。编写产品技术要求时应引用相关适用的国家标准、行业标准,应注意标准编号、标准名称是否完整规范,年代号是否有效;2)合理的引用标准方式。对于适用的强制性标准,产品技术要求中应明确全面执行相关标准,无须引用具体条款。对于推荐性标准,建议在产品技术要求直接引用相关标准及条款号,无须复述标准原文内容。
如有新版强制性国家标准、行业标准发布实施,产品性能指标等要求应执行最新版本的国家标准、行业标准......

站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。
ONE-STOP SERVICE
免费赠送3万家医疗器械企业名录