
发布时间:2021-01-20
附件:医用低温保存箱注册技术审查指导原则(2018年第15号).doc
本指导原则旨在指导注册申请人对第二类医用低温保存箱产品注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。
本指导原则是对医用低温保存箱的一般要求,申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注册申报资料的内容进行充实和细化。
本指导原则是供申请人和审查人员使用的指导文件,不涉及注册审批等行政事项,亦不作为法规强制执行,如有能够满足法规要求的其他方法,也可以采用,但应提供详细的研究资料和验证资料。应在遵循相关法规的前提下使用本指导原则。
本指导原则是在现行法规、标准体系及当前认知水平下制定的,随着法规、标准体系的不断完善和科学技术的不断发展,本指导原则相关内容也将适时进行调整。
一、适用范围
本指导原则所指的医用低温保存箱是一个具有适当容积和装置的绝热箱,箱内温度可控制在-25℃~-164℃温度区间内,用消耗电能的手段来制冷,具有一个或多个间室。
本指导原则仅适用于采用蒸汽压缩式制冷的医用低温保存箱。
处于其他温度范围的医用低温储存设备可参考本指导原则。
根据新《医疗器械分类目录》(国家食品药品监督管理总局公告2017年第104号),分类编码为22(临床检验器械)—15(检验及其他辅助设备)—04(低温储存设备)。
二、技术审查要点
(一)产品名称要求
产品的命名应采用《医疗器械分类目录》或国家标准、行业标准上的通用名称,或以产品结构、控制方式为依据命名,应符合《医疗器械通用名称命名规则》(国家食品药品监督管理总局令第19号)的要求。
建议使用的名称有:低温保存箱、医用低温保存箱、医用冷冻箱等。
(二)产品的结构和组成
医用低温保存箱按门或盖的打开形式可分为顶开式(卧式)和直立式(立式)。
医用低温保存箱一般由围护结构、制冷系统、控制系统、数据记录系统(可选配)及相关附件组成。不同生产企业的产品,在结构上存在一定差异,可不完全与本部分描述一致。
1.围护结构用于医用低温保存箱的存储空间结构的组成及保温。
2.制冷系统用于实现热量的转移,使存储空间内维持所需求的温度环境。
3.控制系统(可包括相应软件及独立电源部分等)用于温度等参数的监控及供电。
4.数据记录系统(可选配)用于箱内温度或存储样品信息等的记录,包括打印机、温度记录仪、电子存储设备等。
5.附件一般包括容器和搁架,也包括需用人工取出的盛物盘等。
(三)产品工作原理/作用机理
1.产品以消耗电能的手段实现热量的转移,从而主动制造出所需的低温环境。
蒸汽压缩式制冷是指液态制冷剂在蒸发器中汽化变成气态制冷剂进入压缩机,被压缩成高温高压的气体,然后排放到冷凝器中,在冷凝器的作用下,气态制冷剂被冷却成高压的液体,然后进入节流装置(常见的有毛细管和膨胀阀),被节流的液态制冷剂的压力和温度再次降低,液态制冷剂进入蒸发器后,会再次汽化吸热,周而复始达到制冷效果。
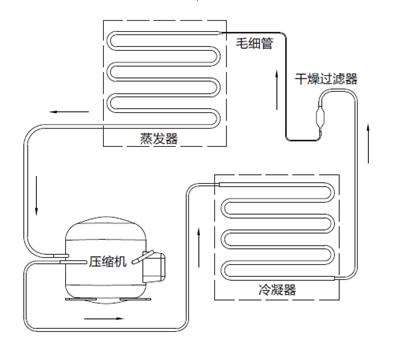
图1 工作原理示意图
2.因该产品为非治疗类医疗器械,故本指导原则不包含产品作用机理的内容。
(四)注册单元划分的原则和实例
注册单元划分一般以产品的技术原理、结构组成、性能指标和适用范围为划分依据。
原则上该指导原则涵盖的产品可划分为同一个注册单元。
(五)产品适用的相关标准
目前与产品相关的国家标准、行业标准列举如下:
表1相关产品标准
| GB/T 191—2008 | 包装储运图示标志 |
| GB 4706.13—2014 | 家用和类似用途电器的安全 制冷器具冰淇淋机和制冰机的特殊要求 |
| GB 4793.1—2007 | 测量、控制和实验室用电气设备的安全要求 第1部分:通用要求 |
| GB/T 14710—2009 | 医用电器环境要求及试验方法 |
| GB/T 18268.1—2010 | 测量、控制和实验室用的电设备 电磁兼容性要求 第1部分:通用要求 |
| GB/T 20154—2014 | 低温保存箱 |
| YY/T 0316—2016 | 医疗器械 风险管理对医疗器械的应用 |
| YY 0466.1—2016 | 医疗器械 用于医疗器械标签、标记和提供信息的符号 第1部分:通用要求 |
上述标准包括了产品经常涉及的标准。有的企业还会根据产品的特点引用一些行业外的标准和一些较为特殊的标准。
产品适用及引用标准的审查可以分两步来进行。首先对引用标准的齐全性和适宜性进行审查,也就是在编写产品技术要求时与产品相关的国家标准、行业标准是否进行了引用,以及引用是否准确。其次对引用标准的采纳情况进行审查。即所引用的标准中的条款要求,是否在产品技术要求中进行了实质性的条款引......

站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。
ONE-STOP SERVICE
免费赠送3万家医疗器械企业名录