
发布时间:2020-12-29
附件:超声多普勒胎儿监护仪注册技术审查指导原则(2017年修订版).doc
本指导原则旨在指导注册申请人对超声多普勒胎儿监护仪产品注册申报资料的准备和撰写,同时也为技术审评部门审评注册申报资料提供参考。
本指导原则系对超声多普勒胎儿监护仪注册技术审查的通用要求,申请人应依据具体产品的特性对注册申报材料的内容进行充实细化。申请人还应依据具体产品的特性确定其中的具体内容是否适用,若不适用,需详细阐述其理由及相应的科学依据。
本指导原则是对产品的技术审查人员和申请人的指导性文件,但不包括注册审批所涉及的行政事项,亦不作为法规强制执行,如果有能够满足相关法规要求的其他方法,也可以采用,但是需要提供详细的研究资料和验证资料。应在遵循相关法规的前提下使用本指导原则。
本指导原则是在当前认知水平下制订的,随着相关法规和标准的不断完善,以及科学技术的不断发展,本指导原则相关内容也将进行适时的调整和更新。审查人员仍需密切关注相关适用标准与注册法规的变化,以确认申报产品是否符合法规要求。
一、适用范围
本指导原则适用于第二类超声多普勒胎儿监护仪,其定义采用YY 0449—2009《超声多普勒胎儿监护仪》3.1,即“由主机、超声探头、宫缩压力传感器及与之相连接的仪器组成,采用超声多普勒原理,具有监测和贮存胎心率、宫缩数据的功能,并可设置报警。”
如果超声多普勒胎儿监护仪作为一个系统中的一部分,则本指导原则也适用于该部分。
本指导原则不适用于超声多普勒胎儿心率仪,该类仪器采用的行业标准为YY 0448—2009《超声多普勒胎儿心率仪》。
二、技术审查要点
(一)产品名称要求
产品的命名应参考《医疗器械通用名称命名规则》(国家食品药品监督管理总局令第19号)和国家标准、行业标准上的通用名称要求。产品名称应以体现产品的工作原理、技术结构特征、功能属性为基本准则,如超声多普勒胎儿监护仪、超声胎儿监护仪,母亲/胎儿综合监护仪等,不宜采用病症命名。
(二)产品的结构和组成
一般由主机、超声探头、宫缩压力传感器及与之相连接的附件组成。一般的结构示意框图如下:
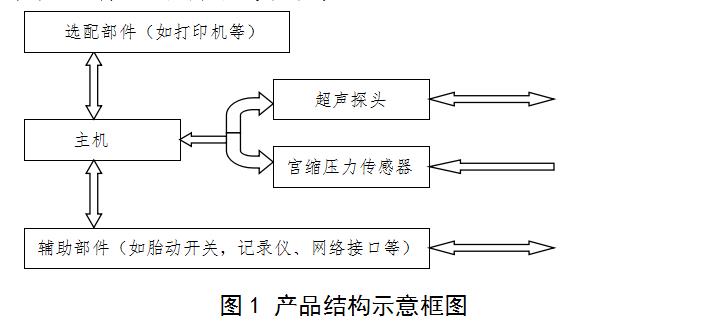
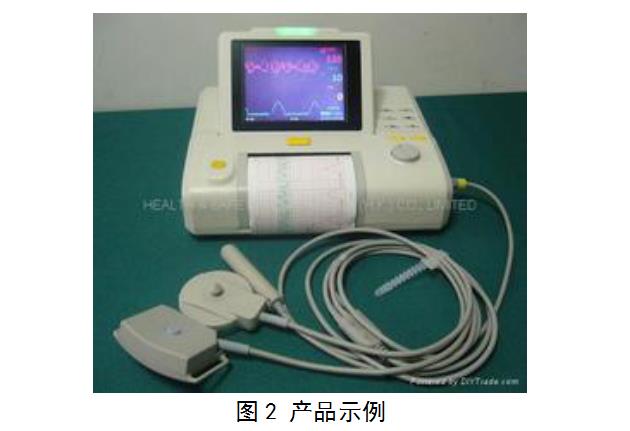
有些设备配有内置打印机的同时,还配有外部打印机或外部打印机接口;显示器也有类似情况。
对超声多普勒胎儿监护仪及其部件进行全面评价所需的基本信息应参考《关于公布医疗器械注册申报资料要求和批准证明文件格式的公告》(国家食品药品监督管理总局公告2014年第43号),包含但不限于以下内容:
1. 产品构成说明
1.1 整机总体构造的描述,应包括所有组成部分,应给出部件的说明(如图表、照片和图纸等),关键部件/组件的说明和标识,其中包括充分的解释来方便理解这些图示。
1.2 对使用者可接触的所有控制装置的说明,包括但不限于:
(1)控制设置范围及在该范围中可能对人体有损害的部分;
(2)缺省值(如果有)。
1.3 产品工作原理框图(应包括所有应用部分,控制部分以及信号输入和输出部分)。
1.4 对所有组件的全面描述,至少包括:
1.4.1 传感器的规格、参数、工作方式。
1.4.2 所有附件、配件的列表。
1.4.3 拟配合使用的设备或部件,并应对接口进行描述。
2. 对产品型号规格的说明以及区别于其他同类产品的特征。
3. 软件研究(如适用)
参见《医疗器械软件注册技术审查指导原则》(国家食品药品监督管理总局通告2015年第50号)的相关要求。
(三)产品工作原理
超声多普勒胎儿监护仪采用超声多普勒原理对孕妇及胎儿进行连续监护,并在出现异常时及时提供报警信息。传感器一般系附在孕妇腹部,通常采用多元扁平超声多普勒换能器。
宫缩的强度通常由压力传感器反馈,进而给出所需的信号。
超声多普勒胎儿监护仪可实时监护胎儿心率等变化情况,为临床提供准确的诊断及处理资料,它既可单独使用,也可通过网络接口与产科中央监护系统连接,形成网络监护系统,也可以同时提供多种移动应用解决方案。
检测胎儿心率信号经处理后将胎儿心率变化趋势用轨迹描记出来,并能同时描记母体的宫缩曲线。
医生根据这二条曲线的变化趋势可以初步判断胎儿的健康状态,以便及时采取措施。
超声多普勒胎儿监护仪所使用的超声波生物物理特性主要......

站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。
ONE-STOP SERVICE
免费赠送3万家医疗器械企业名录