
发布时间:2011-05-11
附件:一次性使用手术衣产品注册技术审查指导原则(食药监办械函[2011]187号).doc
本指导原则旨在指导和规范一次性使用手术衣产品的技术审评工作,帮助审评人员理解和掌握该类产品结构、性能、预期用途等内容,把握技术审评工作基本要求和尺度,对产品安全性、有效性做出系统评价。
本指导原则所确定的主要内容是在目前的科技认识水平和现有产品技术基础上形成的,因此,审评人员应注意其适宜性,密切关注适用标准及相关技术的最新进展,考虑产品的更新和变化。
本指导原则不作为法规强制执行,不包括行政审批要求。但是,审评人员需密切关注相关法规的变化,以确认申报产品是否符合法规要求。
一、适用范围
本指导原则适用于YY0506-2009《病人、医护人员和器械用手术单、手术衣和洁净服》系列标准中的手术衣。手术衣在《医疗器械分类目录》中为第二类医疗器械产品,类代号为6864。
二、技术审评要点
(一)产品名称的要求
产品名称应以预期用途为依据命名,产品名称为一次性使用手术衣。
(二)产品的结构和组成
一次性使用手术衣为手术人员穿着以防止感染原传播的长袍,由前身、后身、袖子、系带等组成。
产品图示举例:
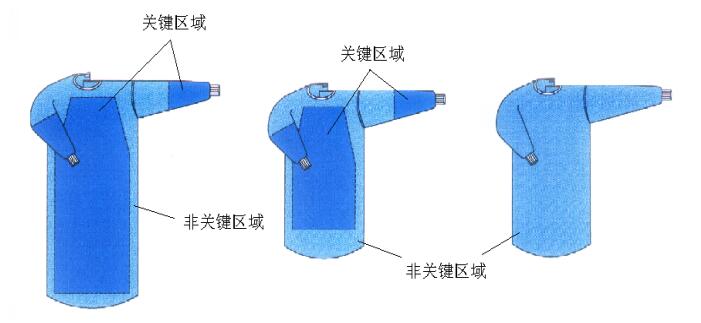
(三)产品适用的相关标准
GB 15980-1995 一次性使用医疗用品卫生标准
GB 18278-2000 医疗保健产品灭菌确认和常规控制要求 工业湿热灭菌
GB 18279-2000 医疗器械 环氧乙烷灭菌确认和常规控制
GB 18280-2000 医疗保健产品灭菌确认和常规控制要求 辐射灭菌
GB/T 16886.1-2001 医疗器械生物学评价 第1部分:评价与试验
GB/T 16886.7-2001 医疗器械生物学评价 第7部分:环氧乙烷灭菌残留量
GB/T 16886.10-2005 医疗器械生物学评价 第10部分:刺激与迟发型超敏反应试验
GB/T 19633-2005 最终灭菌医疗器械的包装
......

站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。
ONE-STOP SERVICE
免费赠送3万家医疗器械企业名录