
发布时间:2022-05-13
一千个人眼里有一千个哈姆雷特,这句莎士比亚的名言,或许也适用于近年临床研究领域当仁不让的热词之一——真实世界研究(RWS)。毕竟,RWS并非严格的概念定义,而是与“药品上市再评价”、“注册登记研究”、“观察性研究”、“横断面研究”、“队列研究”等概念存在着交叉与联系,不同学者有着不同角度的解读。
尽管相关理解和表述有所差异,但RWS的数据特点却是一致的:不再是精准的小样本研究数据,而是混杂的医疗大数据。数据来源广泛复杂,数据质量参差不齐,传统且高昂的人工处理手段捉襟见肘,这无疑给RWS带来了方法学的重大挑战。
为了应对上述挑战,真实世界研究需要多学科专家的合作,这已经成为共识。在这些专家中,有一个人们比较陌生的群体:生物统计学家。对于统计学家的作用,误解之一是将其等同于数据分析。尽管数据分析非常关键,但是良好的研究设计和高效的数据采集模式更加重要。基于此,近日专访了北京大学第一医院医学统计室主任姚晨教授。

万变不离其宗
所谓真实世界研究(RWS),是指在真实的临床、社区或家庭环境下获取多种数据,从而评价某种治疗措施对患者健康真实影响的研究。
众所周知,RWS的概念是针对传统临床试验(RCT)提出的。对此,姚晨教授形象地解释道:“RCT相当于一把枪支在出厂前检查它有没有杀伤力(work or not);但是要想真正检验这把枪能否发挥作用(effective or not),还是要到战场上见真章。临床医生看病不是依靠单一药物或医疗器械,而是基于多种药械和治疗手段的组合,所以真实医疗环境下的数据非常复杂。
因此,RWS可能会用到一些校正已知混杂因素的统计方法(如倾向性评分等),此外与RCT最大的区别在于,RWS无法控制未知的影响因素,所以它得出的结论只能是‘相对’而非‘绝对’的。”
在姚晨看来,RWS并不是一种独立的、新的方法,只是一种“新瓶装老酒”的提法。“统计学从一开始就是研究数据变异的一学门科,如何控制研究过程中各类误差、分析数据变异……方法还是那些方法,不同之处在于随着信息技术的发展,数据记录、储存和传递的方式悄然而变。与之对应的是,RWS的数据采集模式和应用场景也正酝酿着一番变革。”
诚然,我国幅员广阔,患者经济水平差异巨大,真实医疗环境下可以产生的真实世界数据并不意味着一定真实,也完全有可能存在电子病历错漏、失访甚至虚假的问题。如何在不影响临床实践的前提下开展真实世界研究,获取全面且多维度的真实世界研究数据,是目前RWS最为核心的问题。
一方面,如果沿用传统RCT方法,临床研究数据仍依赖临床研究协调员(CRC)的人工录入审核,不仅会导致成本高昂、效率低下,还无法充分保障真实性和准确性——这令人担忧的状况,却是目前国内大部分RWS的真实写照。由于临床研究数据与医疗信息系统的原始记录是脱节而非一体化的,医生可能写的不完整,误写、拷贝粘贴都有可能,数据采集质量也就不言而喻。姚晨表示,上述压力正在推动电子源数据记录工具、远程监查稽查等技术手段的逐渐成熟。
另一方面,如何将真实世界数据(RWD)转化为真实世界证据(RWE),关键要看用到什么程度。如果只是一般的经验总结,也可以叫做RWS;如果需要得出一个科学结论、提出一种研究假设,文章想要发表在专业期刊上,则要对证据产生的过程描述的全面完整;如果是为了将来新产品注册,那就更需要考虑事先研究设计的科学问题、伦理学的合规问题、患者隐私保护的安全问题,涉及临床医学、流行病学、统计学、信息科和医院管理者的多学科通力合作。
科学创新不是一蹴而就的,需要时间的积累。姚晨教授直言,国内即便是率先开展真实世界数据应用试点工作的海南省博鳌乐城国际医疗旅游先行区,尚且还没有完成一个很好的RWS样本案例。尤其对于药械注册审评而言,更强调证据的整合,RWE只是整个证据链中的一环。如何更好与其它循证医学证据评估方法有机结合,如Meta分析、贝叶斯方法等,仍需进一步的研究。
酝酿中的变革
近年来,医疗大数据处理和数据安全技术逐渐成熟,智能化数据采集模式应运而生,尤其是对医院诊疗记录的处理,孕育了不同于传统人工转录誊抄的另一种可能性。
得益于海南博鳌乐城国际医疗旅游先行区在进口药械政策、医疗机构、产品应用场景等方面的聚集效应,又为现代信息技术打通院内诊疗数据的先锋探索提供了肥沃的土壤。
2021年底,《中国食品药品监管》杂志与海南省真实世界数据研究院共建的“真实世界数据研究与药械监管创新”专刊出版,系统介绍了海南博鳌乐城真实世界数据研究成果及案例。其中值得关注的是,姚晨教授团队基于真实世界数据的产生和应用场景,以及满足监管部门的法规要求,构建了一个用于“真实世界数据采集、治理和管理的一体化解决工具”,即电子源数据记录(eSource record,ESR)工具,功能设计主要包含源数据采集、数据提取和治理以及电子数据采集系统对接三部分。如下图所示,将ESR工具应用于多中心临床研究的数据管理创新理念可以类比于当下采用了标准规格的集装箱,让全球的货物可以在世界各地的集装箱码头实现自动化运输和管理。
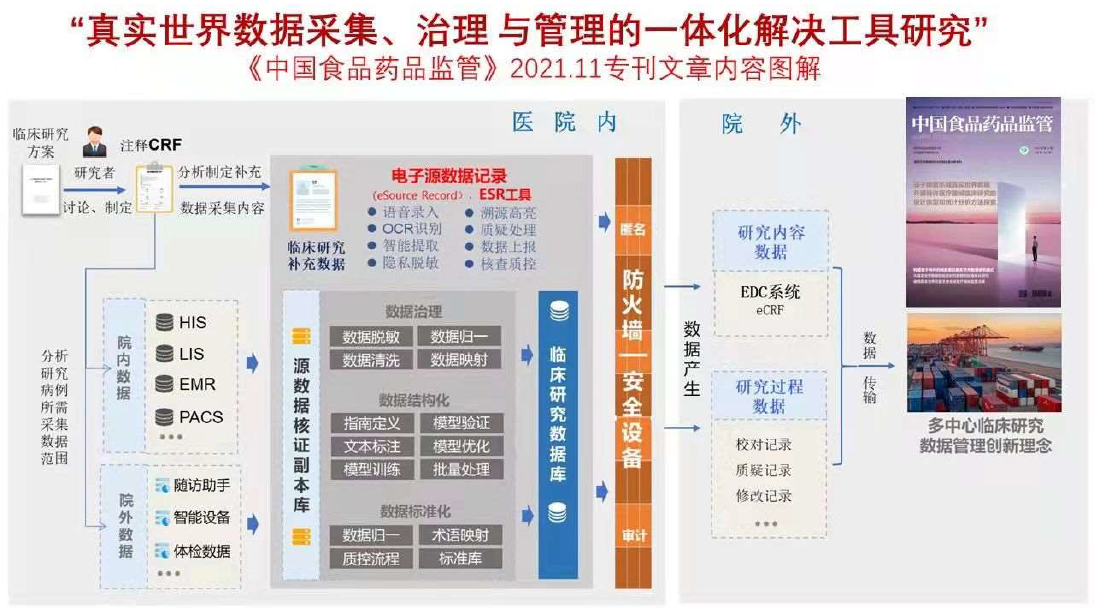
为了评估ESR在临床实践中的应用效果,姚晨教授团队在博鳌一龄生命养护中心进行了ESR工具的部署和真实世界数据研究项目的试用。测试结果发现:以传统临床研究流程作为对比,基于ESR的eSource方式能提高源数据的采集效率,减少完成数据转录所需的工作量。这项研究成果证明了ESR的可行性和应用价值。整体实践的详细研究成果已经发表在英国《BMC MedicalInformatics and Decision Making》杂志。
据介绍,目前ESR工具在内地医院的试点工作正在逐步推广之中,包括罕见病多学科会诊记录和医疗机构研究者发起的临床研究数据管理工作等。
“大家可能会问:RWS不能通过随机和盲法来控制变异,如何保障研究结果的可信度?”姚晨教授对真实世界研究的短板毫不避讳:“我们更强调的是把各种混杂因素记录下来,再利用统计方法来校正偏倚。比方说已知混杂因素的校正,现在用的比较多的叫倾向性评分,就是把病人的基本情况、伴随疾病治疗和生活环境因素等记录下来,通过计算的倾向性得分匹配保证分析组间的相对均衡性。但是这样一来,也可能有样本量的损失。”
“所以RWS需要的样本量是比较大的,而且是更多维度的数据,”姚晨教授补充道:“我们不要一提到大数据,就是大样本量,实际上更多维度的数据才是大数据。为什么?你没有记录下其他重要的混杂因素,任何统计学家也没办法。虽然现在也有一些方法学进展,比如工具变量的应用,但这些应用依然还是受到一些条件限制的。所以我个人觉得,最简单最好的办法,就是根据研究方案的要求尽可能完善的记录这些数据,然后进行多因素的分析,去探讨潜在的规律。”
“如果完全依靠人工的方法,这是不现实的,现代信息技术是一个解决当下数据质量问题的非常有前景的应用方向,”姚晨教授进一步解释道:“通过语音自动转化文字和自然语言识别技术(NLP),可以在不影响医生诊疗行为的前提下,快速准确的记录数据并进行结构化处理。与过去RCT根据研究方案要求填写病例报告表(CRF)一样;RWS也需要根据研究方案的要求去获取最原始、最真实的源数据,然后再用NLP技术加以提取和审核校验,从而提高效率。”
与此同时,数据标准化的需求和挑战也不容忽视。“真实世界数据和临床研究数据标准是不一样的,我们不可能要求统一,但应该有一套两个数据标准之间互相映射和转化的过程。”
针对这一难点问题,姚晨教授团队探索和设计出了一套对数据进行标准化的方法,可以用于实现从EMR源数据,自动填充满足临床数据交换标准协会(CDISC)标准的电子病例报告表格(eCRF),并满足监管部门的数据递交要求。据悉,目前研究结果“从真实世界数据到临床研究数据的标准转化研究”已经在《中国食品药品监管》杂志2021年11月专刊发表。
在姚晨看来,数据递交标准的统一是一种国际化的大趋势。一旦实现,监管机构在审阅各种统计报告的时候就可以进行数据合并和模型比较,带来审批时间上的缩短;还可以方便统计师的各种模型应用;将来数据共享的时候也有很大的意义,有效避免各自为政。
采访的尾声,姚晨教授表示,真实世界研究由于其方法学的局限性,不可能像RCT得出一个直接效应的评估,更多是间接效益评估,为进一步的研究提出合理的假设。我们需要保持清醒的头脑,客观评价目前阶段性的成果,正视数据质量和标准化的瓶颈问题。简而言之,清晰明确的数据收集和质量控制过程是实现研究结论的合理性和可靠性的保障,相信统计学家和临床医学专家之间越来越多的交流与合作,必将促进临床研究的创新和发展!

站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。
ONE-STOP SERVICE
免费赠送3万家医疗器械企业名录