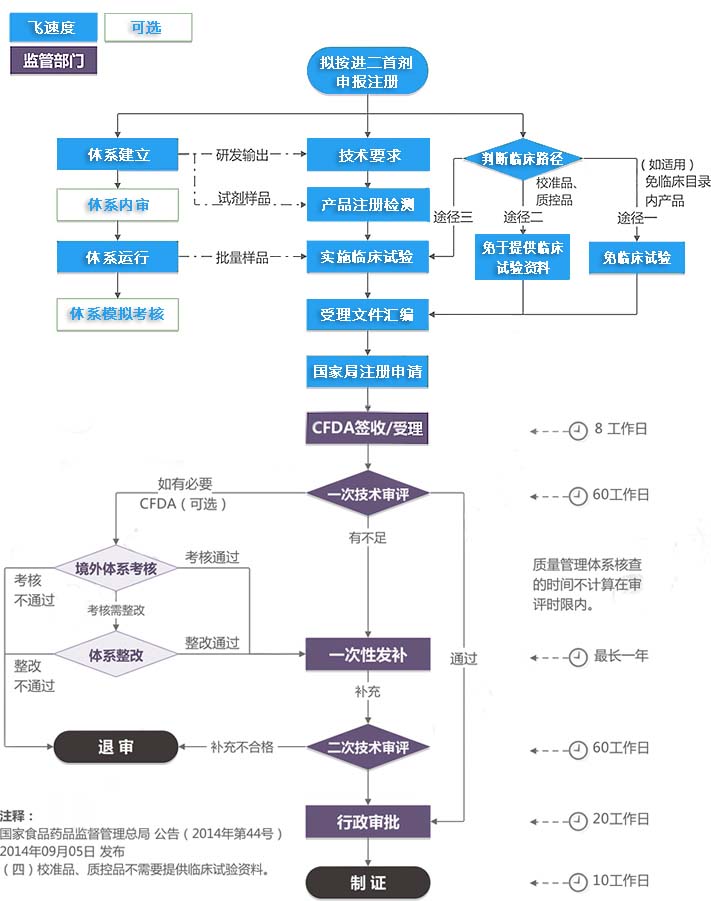
依据《
体外诊断试剂注册管理办法》(局令5号)第六条规定:进口第二类体外诊断试剂由药监总局审查,批准后发给
医疗器械注册证。向我国境内出口第二类医疗器械的境外生产企业,应当由其在我国境内设立的代表机构或者指定我国境内的企业法人作为代理人,向药监管理部门提交注册申请资料和注册申请人所在国(地区)主管部门准许该医疗器械上市销售的证明文件,不属于医疗器械产品也需上市销售证明。注册代理人承担责任增加了协助召回和售后连带责任。
进口二类IVD产品首次注册办事条件
申请人应为境外生产企业,且该医疗器械已在注册申请人注册地或者生产地址所在国家(地区)已获准上市销售。
申请材料清单
1、申请表;
2、证明性文件;
3、综述资料;
4、分析性能评估资料;
5、阳性判断值或参考区间确定资料;
6、稳定性研究资料;
7、生产及自检记录;
8、临床评价资料;
9、产品风险分析资料;
10、产品技术要求;
11、产品注册检验报告;
12、产品说明书;
13、标签样稿;
14、符合性声明。
15、主要原材料的研究资料;
16、主要生产工艺及反应体系的研究资料;
注意:15、16两项,注册申请时不需要提供,由申报单位保存,如技术审评需要时提供。
境外申请人应当提交的资料
1、申请人注册地或生产地址所在国家(地区)医疗器械主管部门出具的允许产品上市销售的证明文件和可以合法生产申报产品的资格证明文件,如该证明文件中有产品类别描述,其类别应当覆盖申报产品。
2、申请人注册地或者生产地址所在国家(地区)未将该产品作为医疗器械管理的,申请人需要提供相关证明文件,包括注册地或者生产地址所在国家(地区)准许该产品上市销售的证明文件。
3、申请人符合注册地或者生产地址所在国家(地区)医疗器械生产管理质量体系要求或者通过其他质量管理体系认证的证明文件。
4、申请人在中国境内指定代理人的委托书、代理人承诺书及营业执照副本复印件或者机构登记证明副本复印件。